
【题目】M、W、X、Y、Z是同周期主族元素,X原子的最外层电子数是W原子次外层电子数的3倍。它们形成的化合物可用作新型电池的电极材料,结构如图所示,化合物中除![]() 外其它原子均满足8电子稳定结构。下列说法正确的是
外其它原子均满足8电子稳定结构。下列说法正确的是
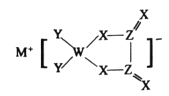
A.M的单质通常保存在煤油中B.W的最高价氧化物对应的水化物是一元弱酸
C.简单气态氢化物稳定性X>YD.上述五种元素中Z的电负性最大
【答案】B
【解析】
M、W、X、Y、Z是同周期主族元素, X的最外层电子数是W次外层电子数的3倍, W有两个电子层,次外层为2个电子, X为O元素,由盐的结构可知,Z可以形成四个共价键,且能与氧形成双键,因此Z的最外层电子数为4 ,Z为C元素;四种元素位于同周期,且Y能形成一个共价键,Y为F元素; W能形成4个共价键,W为B元素;新型电池材料,除M外均满足8电子稳定结构,M形成+1价离子,M为Li元素;故M为Li元素, X为O元素, Y为F元素,Z为C元素,W为B元素。
A.M为Li元素,Li单质密度比煤油小,不可以保存在煤油中,一般保存在石蜡油中,A错误;
B.W为B元素,W的最高价氧化物对应的水化物为H3BO3为一元弱酸,B正确;
C.同周期元素非金属性从左到右依次增大,所以非金属性F>O,非金属性越强,气态氢化物的稳定性越强,故稳定性HF>H2O,C错误;
D.同周期从左到右元素的电负性逐渐增大,上述五种元素中,F的电负性最大,D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】![]() 资源化利用的方法之一是合成二甲醚(
资源化利用的方法之一是合成二甲醚(![]() 简写做
简写做![]() )。
)。![]() 催化加氢法合成
催化加氢法合成![]() ,其过程中主要发生下列反应:
,其过程中主要发生下列反应:
反应Ⅰ:![]()
![]()
反应Ⅱ:![]()
![]()
其中,反应Ⅱ分以下两步完成,请写出反应Ⅳ的热化学方程式。
反应Ⅲ:![]()
![]()
反应Ⅳ:___________。
⑴反应Ⅳ的热化学方程式为________。
⑵在![]() 和
和![]() 的起始量一定的条件下,
的起始量一定的条件下,![]() 的平衡转化率和平衡时
的平衡转化率和平衡时![]() 、
、![]() 的选择性随压强或温度的变化见下图。已知:
的选择性随压强或温度的变化见下图。已知:
![]() 的选择性
的选择性![]() ;
;
![]() 的选择性
的选择性![]()
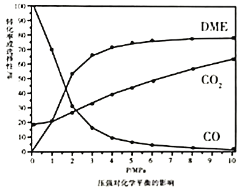
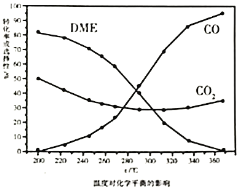
①依据图像中的数据分析,提高平衡时![]() 的选择性应当选择的条件为________。
的选择性应当选择的条件为________。
A 高温高压 B 低温低压 C 高温低压 D 低温高压
按照温度对化学平衡的影响图像分析温度低于300℃,![]() 平衡转化率随温度升高而降低的原因是_______。
平衡转化率随温度升高而降低的原因是_______。
②某温度和压强下,起始投入![]() 与足量
与足量![]() 发生反应,达到平衡时
发生反应,达到平衡时![]() 的转化率为40%,部分物质的物质的量如下表:
的转化率为40%,部分物质的物质的量如下表:
|
|
|
|
|
|
计算平衡时![]() 的选择性为________,反应Ⅳ的化学平衡常数为________。
的选择性为________,反应Ⅳ的化学平衡常数为________。
⑶经研究发现,在不同反应条件下反应相同时间(未平衡)测定发现,体系中![]() 的浓度均很低,则可知活化能大小关系:反应Ⅲ________反应Ⅳ(填“大于”、“小于”或“等于”)。
的浓度均很低,则可知活化能大小关系:反应Ⅲ________反应Ⅳ(填“大于”、“小于”或“等于”)。
⑷![]() ,投料比为
,投料比为![]() 时进行反应,
时进行反应,![]() 的浓度随时间变化如下图所示,则下列说法正确的为________。
的浓度随时间变化如下图所示,则下列说法正确的为________。
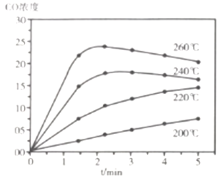
A 在![]() 范围内,反应Ⅰ的速率随温度升高而增大
范围内,反应Ⅰ的速率随温度升高而增大
B 200℃条件下,随反应时间的延长,![]() 的浓度始终增大
的浓度始终增大
C 260℃条件下,随反应时间的延长,![]() 的浓度先增大后减小最终不变
的浓度先增大后减小最终不变
D 260℃条件下,![]() 后
后![]() 的浓度减小是因为随时间推移反应Ⅱ的进行使体系中
的浓度减小是因为随时间推移反应Ⅱ的进行使体系中![]() 浓度越来越高,反应Ⅰ的逆反应速率不断增大,从而使
浓度越来越高,反应Ⅰ的逆反应速率不断增大,从而使![]() 浓度逐渐下降
浓度逐渐下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示[已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJ·mol-1:请回答下列问题:
2SO3(g) ΔH=-196.6kJ·mol-1:请回答下列问题:
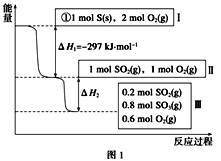
(1)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比|ΔH2|___(填“大”、“小”或“相等”)。
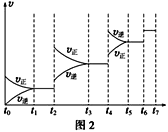
(2)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___;图中表示平衡混合物中SO3的含量最高的一段时间是____。
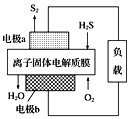
(3)科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。则电极b上发生的电极反应为___;电路中每通过4mol电子,在负极消耗___L(标况)气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+n(B)(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
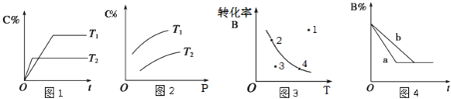
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n<p
C.图3中,表示反应速率v(正)>v(逆)的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为定性探究乙醇的分子结构,某化学课外小组设计了如下实验方案:在盛有金属钠粒的烧瓶中,用分液漏斗慢慢加入无水乙醇(如图所示),点燃放出的气体,并把一干燥的小烧杯罩在火焰上,在烧杯壁上出现液滴后,迅速倒转烧杯,向烧杯中加入少量的澄清石灰水,观察有无混浊。

(1)以上实验设计存在重大安全隐患,请你帮他们指出来_______________________ ;
(2)确认所用乙醇为无水乙醇的方法是______________________________________ ;
(3)若向烧杯中加入少量澄清石灰水后发现有混浊,那么燃烧产生二氧化碳的物质最可能是_____________ ;
(4)若向烧杯中加入少量澄清石灰水后未发现混浊,则可推断乙醇分子结构中含有______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知6.2克某有机物在氧气中完全燃烧,其产物(100 ℃)依次通过盛有浓硫酸的洗气瓶、盛有碱石灰的干燥管全部被吸收后,洗气瓶的质量增加5.4克,干燥管的质量增加8.8克。
(1)计算确定该有机物的最简式。_________________
(2)相同条件下,若该有机物蒸气相对氢气的密度为31,计算确定该有机物的分子式。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:P4(g)+6Cl2(g)=4PCl3(g) ΔH=a kJ·mol-1,Cl—Cl键的键能为bkJ·mol-1,PCl3中P—Cl键的键能为ckJ·mol-1,P4的结构为![]() 。则P—P键的键能为
。则P—P键的键能为
A.(a-6b+12c)/6kJ·mol-1B.(a-3b+12c)/4kJ·mol-1
C.(a-6b-12c)/6kJ·mol-1D.(a-3b-12c)/4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学平衡移动的分析中,正确的是
A.平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),当增加反应物的物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物的物质的量时,平衡一定向正反应方向移动
B.已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率降低
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率降低
C.有气体参加的反应达到平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
D.有气体参加的反应达到平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。下列叙述正确的是( )
A.偏二甲肼的摩尔质量为60 g
B.6.02×1023个偏二甲肼分子的质量约为60 g
C.1 mol偏二甲肼的质量为60 g·mol-1
D.6 g偏二甲肼含有NA个偏二甲肼分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com