
| A. | 有机物中都存在同分异构现象 | |
| B. | 14C和14Si是同位素 | |
| C. | C2H5Cl没有同分异构体 | |
| D. | 只要含有的官能团种类相同就是同系物 |
分析 A、不是所有有机物均存在同分异构现象;
B、同位素是质子数相同,中子数不同的原子;
C、分子式相同,结构不同的有机化合物互称同分异构体;
D、同系物中官能团种类相同,且数目相同.
解答 解:A、不是所有有机物均存在同分异构现象,比如甲烷、乙烷、丙烷、甲醇等均不存在同分异构体,故A错误;
B、14C和14Si的质子数不同,不是同位素,故B错误;
C、C2H5Cl只有一种结构,没有同分异构体,故C正确;
D、官能团种类相同不一定是同系物,如乙二醇与丙醇.故D错误,
故选C.
点评 本题考查了有机物的结构、同系物的概念、同分异构,题目难度不大,注意把握概念的内涵与外延,可以采用举例法来分析.


科目:高中化学 来源: 题型:选择题
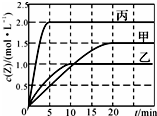 向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( )
向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( ) | 容器 | 甲 | 乙 | 丙 | |
| 容积/L | 0.5 | 0.5 | 1.0 | |
| 温度/℃ | T1 | T2 | T2 | |
| 反应物起始量 | 1.0 mol X 0.5 mol Y | 1.0 mol X 0.5 mol Y | 4.0 mol X 2.0 mol Y |
| A. | 该反应温度升高,平衡常数减小 | |
| B. | 20 min内甲容器中反应的平均速率:v(X)=0.0375mol•(L•min)-1 | |
| C. | 10 min时,其他条件不变,向乙容器中再加入2 mol Z,平衡向逆反应方向移动 | |
| D. | 其他条件不变,若缩小乙的体积,Y的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸 纯碱 硫酸钙 | |
| B. | 氢氯酸 烧碱 硫酸亚铁 | |
| C. | 碳酸 乙醇 烧碱 | |
| D. | 磷酸 熟石灰 苛性钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是最早使用的半导体材料 | B. | 盛NaOH溶液的试剂瓶塞可用玻璃塞 | ||
| C. | 水泥、玻璃、水晶都是硅酸盐制品 | D. | 自然界中没有单质硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液+AgNO3溶液→生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液+BaCl2溶液→生成白色沉淀,说明原溶液中有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 某溶液+稀硫酸→生成无色气体,该气体能使澄清石灰水变浑浊,则原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
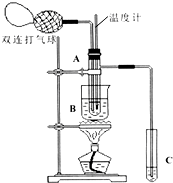 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com