
【题目】Ⅰ:用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:

实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
② | 20 mL 0.2 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
(1)该实验探究的是_________________________________因素对化学反应速率的影响。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________ mol·L-1(假设混合溶液的体积为50 mL)。
(3)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:
①产物Mn2+是反应的催化剂,②_______________________________
Ⅱ:当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式为___________________________________
(2)在恒温恒容密闭容器中,判断上述反应达到平衡状态的依据是________________
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1
【答案】浓度0.0052反应放热,温度升高2CO2+6H2![]() C2H5OH(g)+3H2O(g)ab
C2H5OH(g)+3H2O(g)ab
【解析】
Ⅰ:(1)对比①②实验可知,探究的是浓度对化学反应速率的影响,故答案为:浓度;
(2)CO2的物质的量是:4.48mL×10-322.4mol/l=0.0002mol,设2min末,反应的MnO4-的物质的量为X,
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2 10
X 0.0002mol
解得 X=0.00004mol,30mL×10-3×0.01molL-1-0.00004mol=0.00026mol,c(MnO4-)=nv=0.00026mol0.05L=0.0052mol/L,故答案为:0.0052;
(3)影响化学反应速率的因素主要有温度、浓度、压强和催化剂,除催化剂之外,只能是温度升高导致反应速率加快,故答案为:该反应放热使反应温度升高;
Ⅱ:(1)当温度高于500K时,科学家成功利用二氧化碳和氢气合成了1mol乙醇和水,该反应的化学方程式为:2CO2+6H2CH3CH2OH(g)+3H2O(g),故答案为:2CO2+6H2CH3CH2OH(g)+3H2O(g);
(2)a.该反应中混合气体的物质的量减小,则体系压强一直在减小,当体系压强不再改变,能说明到达平衡,故a正确;b.H2的浓度不再改变,说明正逆反应速率相等,该反应达到平衡状态,故b正确;c.容器的体积不变,混合气体的质量不变,混合气体的密度始终不变,气体的密度不随时间改变,不能说明到达平衡,故c错误;d.单位时间内消耗H2和CO2的物质的量之比为3:1,指正反应方向,无法判断正逆反应速率是否相等,则不能说明到达平衡,故d错误;故答案为:ab。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】已知25℃时,K=![]() =1.75×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是( )
=1.75×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是( )
A.向该溶液中加入一定量的硫酸,K增大
B.升高温度,K增大
C.向CH3COOH溶液中加入少量水,K增大
D.向CH3COOH溶液中加入少量氢氧化钠溶液,K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素为地壳中含量最高的元素,可形成多种重要的单质和化合物。
(1)氧元素位于元素周期表中___________区;第二周期元素中,第一电离能比氧大的有___________种。
(2)O3可用于消毒。O3的中心原子的杂化形式为___________;其分子的 VSEPR模型为___________,与其互为等电子体的离子为___________(写出一种即可)。
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为___________;C2H5OH不能用无水CaCl2千燥是因为Ca2+和C2H5OH可形成[Ca(C2H5OH)4]2+,该离子的结构式可表示为______________________。
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为___________;与O2-紧邻的所有Fe2+构成的几何构型为___________。
②Cu2O立方晶胞结构如图2所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为___________g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池已用于航天飞机,其工作原理如图所示。关于该燃料电池的说法不正确的是
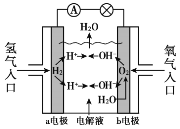
A. H2在负极发生氧化反应
B. 电子从a电极经外电路流向b电极
C. 供电时的总反应为:2H2 + O2 == 2H2O
D. 燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含碳化合物的结构与性质,对生产、科研等具有重要意义。
(1)某同学画出基态碳原子的核外电子排布图:![]() ,该电子排布图违背了__;CH3+、-CH3、CH3-都是重要的有机反应中间体。CH3+、CH3-的空间构型分别为___、____。
,该电子排布图违背了__;CH3+、-CH3、CH3-都是重要的有机反应中间体。CH3+、CH3-的空间构型分别为___、____。
(2)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。
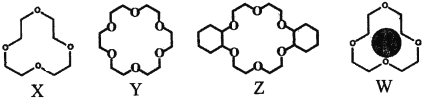
①Li+与X的空腔大小相近,恰好能进入到X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。基态锂离子核外能量最高的电子所处能层符号为___________;
②冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构。理由是___________。
③烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶入冠醚Z,氧化效果明显提升。
i.水分子中氧的杂化轨道的空间构型是___________,H-O键键角___________(填“>”“<”或“=”)109°28′
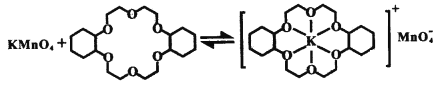
ii.已知:冠醚Z与KMnO4可以发生下图所示的变化。加入冠醚Z后,烯烃的氧化效果明显提升的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要有机化工原料。结合以下路线回答:
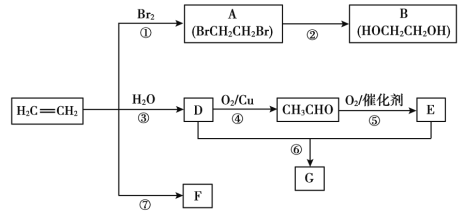
已知:2CH3CHO + O2催化剂,加热2CH3COOH
(1)反应①的化学方程式是_______。
(2)B的官能团是_______。
(3)F是一种高分子,可用于制作食品袋,其结构简式为_______。
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,装置如图所示。

i.反应⑥的化学方程式是______,反应类型是_____。
ii.分离出试管乙中油状液体用到的主要仪器是_______。
制法二:工业上用CH2=CH2和E直接反应获得G。
iii.反应类型是___。
iv.与制法一相比,制法二的优点是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
A.19种 B.9种 C.15种 D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),结合下图回答问题。
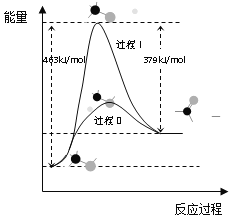
①此反应的热化学方程式是______
②反应活化能:过程I___过程II(填“>”“=”或“<”)
③过程II温度—转化率图如下,下列说法合理的是_____
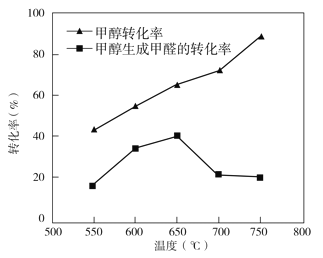
a.甲醇脱氢法制备甲醛过程无副反应发生
b.温度高于 650℃催化剂烧结,活性减弱
c.及时分离产品有利于提高甲醇生成甲醛的转化率
(2)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。
①某甲醛气体传感器的工作原理如图所示,b极的电极反应式为____,当电路中转移4×10-4 mol电子时,传感器内参加反应的甲醛(HCHO)为_____mg。

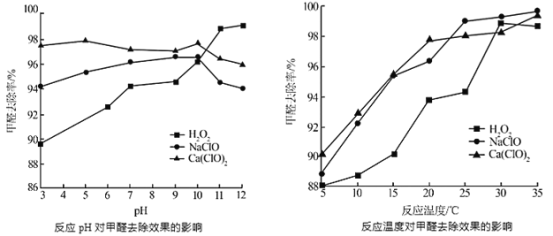
②氧化剂可处理甲醛污染,结合以下图像分析春季(水温约15℃)应急处理甲醛污染的水源应选择的试剂为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2可用于电子、仪表等工业。以毒重石(主要成分为BaCO3,含少量的CaCO3、MgSO4、Fe2O3、SiO2等杂质)为原料,模拟工业制取BaCl2·2H2O的流程如下图所示:

已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(1)盐酸浸取时需要适当加热的原因是_________。
(2)用37%的盐酸配制15%的盐酸需用到的仪器有________(填字母)
A.量筒 B.烧杯 C.容量瓶 D.玻璃棒
(3)滤渣I的成分为__________;
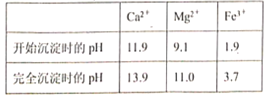
(4)Mg(OH)2的溶度积常数Ksp=_______,加入H2C2O4时发生的离子反应为_______,加入H2C2O4应避免过量,其原因是_________。
(5)母液中除了含有Ba2+、Cl—外,还含有大量的_________(填离子符号);
(6)滤渣III(不含结晶水)是结石的主要成分滤渣Ⅲ经过洗涤干燥后在空气中进行热重分析,取128.0g该纯净物,在200~470℃灼烧,最后得到100.0g产物,200~470℃时发生反应的化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com