
【题目】孔雀石主要含Cu2(OH)2CO3 , 以及少量Fe、Si的化合物.可以用孔雀石为原料制备胆矾(CuSO45H2O),步骤如图: 
请回答下列问题:
(1)试剂①是一种常见的酸,写出其化学式 . 过滤所需要的玻璃仪器有
(2)实验室检验Fe3+的常用方法是 .
(3)溶液A中的金属离子有Cu2+、Fe2+、Fe3+ , 上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+ , 从而形成溶液B,则试剂②能否用氯水(填“能”或“不能”,若“不能”,请解释原因).
(4)由溶液C获得胆矾,需要经过、、过滤等操作.
(5)取25.00mL溶液A,用1.000×10﹣2mol/LKMnO4标准溶液滴定.反应离子方程式为:5Fe2++MnO4﹣+8H+→5Fe3++Mn2++4H2O,若消耗标准溶液20.00mL,则溶液A中Fe2+的浓度为 .
【答案】
(1)H2SO4;漏斗、烧杯、玻璃棒
(2)取样,向其中滴加KSCN溶液,溶液变血红色,则含有Fe3+
(3)不能,如加氯水会引入杂质Cl﹣
(4)蒸发浓缩;冷却结晶
(5)0.040mol/L
【解析】解:(1)试剂①是一种常见的酸,应为硫酸,最终得到硫酸铜,以避免引入新杂质,过滤所需要的玻璃仪器有漏斗、烧杯、玻璃棒,
所以答案是:H2SO4;漏斗、烧杯、玻璃棒;(2)检验铁离子,可取样,向其中滴加KSCN溶液,溶液变血红色,则含有Fe3+,所以答案是:取样,向其中滴加KSCN溶液,溶液变血红色,则含有Fe3+;(3)不用加入氯水,否则生成氯化铜而引入新杂质,所以答案是:不能,如加氯水会引入杂质Cl﹣;(4)由溶液C获得胆矾,需要经过蒸发浓缩、冷却结晶、过滤等操作,所以答案是:蒸发浓缩;冷却结晶;(5)n(KMnO4)=1.000×10﹣2mol/L×0.02L=2.000×10﹣4mol,离子方程式为:5Fe2++MnO4﹣+8H+→5Fe3++Mn2++4H2O,可知n(Fe2+)=1.000×10﹣3mol,
则溶液A中Fe2+的浓度为 ![]() =0.040mol/L,
=0.040mol/L,
所以答案是:0.040mol/L.


科目:高中化学 来源: 题型:
【题目】实验室用NH4Cl和Ca(OH)2制取氨气,下图A和B是常用的气体发生装置。

(1)实验室制氨气时反应的化学方程式是______________________________________,应选用的装置是_____;若改用浓氨水和NaO固体制氨气时,应选取的装置是________。
(2)为了得到干燥的氨气,实验室常使用________做干燥剂(请从碱石灰、浓硫酸、氯化钠中选出一种物质)。
(3)实验室常用_______法收集氨气。在标准状况下,将盛满氨气的集气瓶倒置于水中(假设溶质全部在集气瓶内),则所得溶液的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是( ) 
A.布洛芬的分子式为C13H18O2
B.布洛芬与苯乙酸是同系物
C.1mol 布洛芬最多能与3mol 氢气发生加成反应
D.布洛芬在苯环上发生取代反应,其一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面两种方法可以制得白色的Fe(OH)2沉淀:
【方法一】用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应来制备。
实验室用硫酸亚铁晶体配制上述FeSO4溶液时,一般需加入铁粉和稀硫酸,加入铁粉的目的是_____________。
【方法二】在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂来制备。

(1)实验开始时,止水夹e是______(填“打开”或“关闭”)的。
(2)如何检验装置内空气已经排尽?________________。
(3)排尽装置内空气后,为了制得白色Fe(OH)2沉淀,操作步骤是________。
(4)开启活塞f放掉约2/3液体,此时裝置B中试剂瓶中发生的化学反应方程式为________。
(5)下列各图示中________(填序号)能较长时间看到Fe(OH)2白色沉淀。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Fe2+、Mg2+、Cu2+、NH4+、A13+、OH-、SO42- 中的一种或几种。当加入一种淡黄色固体并加热溶液时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。请填写下列空白:
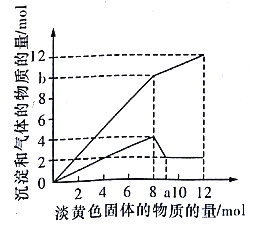
(1)图中a点的值是__________;所加的淡黄色固体是_________ (填化学式)。
(2)该溶液中含有的离子是_________。
(3)如何检验溶液中存在的阴离子? _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究苯和溴反应的反应原理,特进行如下实验,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉. 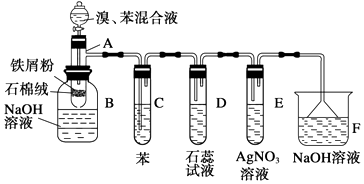
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):
(2)试管C中苯的作用是 . 反应开始后,观察D的现象为E的现象为
(3)整套装置中,具有防倒吸作用的仪器有(填字母).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应aFeCl2+bKNO3+cHCl=- dFeCl3+eKCl+fX+gH2O中,其中a,b,c,d,e,f,g均为相应的物质系数,若b=l.d=3,则生成物X的分子式为
A. NO2 B. NO C. N2O D. NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl26H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3 , 还含少量Fe2O3、Al2O3、MnO等)制取CoCl26H2O的工艺流程如图1: 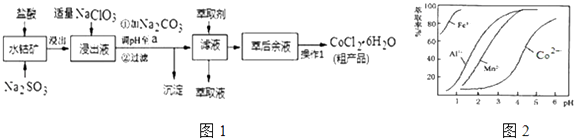
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl26H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式 .
(2)写出NaClO3发生反应的主要离子方程式;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 .
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为 .
(4)制得的CoCl26H2O在烘干时需减压烘干的原因是 .
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是;其使用的最佳pH范围是 . A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl26H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl26H2O的质量分数大于100%,其原因可能是 . (答一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com