
����Ŀ��������Ԫ��W��X��Y��Z�����ڱ��е����λ�������ʾ��������Ԫ��ԭ�ӵ�����������֮��Ϊ21���ش��������⣺
W | X | |||
Y | Z |
��1������Ԫ�ؼ����ӵİ뾶�ɴ�СΪ_____________�������ӷ��ű����
��2��W������⻯��ĵ���ʽΪ________________��
��3��W��X���⻯���зе�ϸߵ���___________���ѧʽ����
��4��Y������Fe2O3��Ӧ�ܷų��������ȣ������ں��Ӹֹ죬�÷�Ӧ��ѧ����ʽΪ________��
��5����ʢ��3 mL��������Һ���Թ�����뼸��W������������ˮ����Ũ��Һ��ʵ������Ϊ_________��
��6������ʽΪC4H9Z���л�����ͬ���칹����_____�֡�
���𰸡�Cl-��N3-��O2-��Al3��![]() H2O2Al��Fe2O3
H2O2Al��Fe2O3![]() 2Fe��Al2O3������ɫ����(��ɫ��������)4
2Fe��Al2O3������ɫ����(��ɫ��������)4
��������
��Wԭ�ӵ�����������Ϊx����ͼ����֪������Ԫ��ԭ�ӵ�����������֮�ͣ�x+x+1+x-2+x+2��21�����x��5����WΪNԪ�ء�XΪOԪ�ء�YΪAlԪ�ء�ZΪClԪ�أ��ݴ˽��
�������Ϸ�����֪WΪNԪ�ء�XΪOԪ�ء�YΪAlԪ�ء�ZΪClԪ�أ���
��1�����ӵĺ�����Ӳ���Խ�࣬���Ӱ뾶Խ��������Ų���ͬʱ���Ӱ뾶��ԭ���������������С��������Ԫ�ؼ����ӵİ뾶�ɴ�СΪCl-��N3-��O2-��Al3����
��2��W������⻯���ǰ���������ʽΪ![]() ��
��
��3��ˮ���Ӽ�����ǿ�ڰ������Ӽ�����������W��X���⻯���зе�ϸߵ���H2O����������Һ̬������������̬��
��4����������Fe2O3�������ȷ�Ӧ���ܷų��������ȣ������ں��Ӹֹ죬�÷�Ӧ��ѧ����ʽΪ2Al��Fe2O3![]() 2Fe��Al2O3��
2Fe��Al2O3��
��5��Ũ������ʹ�����ʱ��ԣ�����ʢ��3 mL��������Һ���Թ�����뼸��W������������ˮ����Ũ��Һ��ʵ������Ϊ������ɫ����(��ɫ��������)��
��6�����ڣ�C4H9��4�ֲ�ͬ�Ľṹ�������ʽΪC4H9Cl���л�����ͬ���칹����4�֡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2Ϊ������Ⱦ��о��������ʶԻ�������������Ҫ���塣����������ͭ������ʱ����������Ȼ���ѳ������������յ������۵�Ϊ112.8�棬�е�Ϊ444.6�棩��

��1����װ���е���X�������ǣ�______________________________��
����װ��A��ȡSO2�����Լ�����������_________������ĸ����
a. 18.4 mol/L H2SO4��Cu b. 4 mol/L HNO3��Na2SO3 c. 60% H2SO4��K2SO3
��ˮ��Al4C3��װ��A����ȡ���飬�仯ѧ����ʽΪ��_______________________________��
��2�������Ƶõ�CH4��SO2�����B��Gװ����֤��Ӧ���CH4��2SO2![]() 2S��CO2��2H2O���ɵĵ���S��CO2��
2S��CO2��2H2O���ɵĵ���S��CO2��
��Bװ�����������ã��ֱ���_________��__________��__________��
��ʵ��װ���������ӵĺ���˳��ΪB��_____________________��ÿ��װ��ֻ��һ�Σ���
��֤����CO2����������Ϊ_____________________________��
��Gװ���з�����Ӧ�����ӷ���ʽΪ_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ��ȷ�ӦH2 + Cl2 ![]() 2HCl����˵������ȷ����
2HCl����˵������ȷ����
A. �÷�Ӧ��,��ѧ��ֻת��Ϊ����
B. ��Ӧ�������е����������ڲ��������е�������
C. ���������е����������ڷ�Ӧ�������е�������
D. �Ͽ�1mol H-H����1mol Cl-Cl�������յ�������С���γ�2mol H-Cl�����ų�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����á� Na��CO2����ؽ�CO2���Ϊ�����ҹ�������Ա���Ƴ��Ŀɳ�硰Na��CO2����أ����Ʋ��Ͷ��̼����(MWCNT)Ϊ�缫���ϣ��ŵ練Ӧ����ʽΪ4Na��3CO2 ��2Na2CO3��C���ŵ�ʱ�õ�ء����롱CO2���乤��ԭ����ͼ��ʾ������˵���д�����ǣ� ��
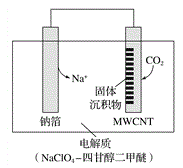
A. ��������Ϊ��MWCNT�����ߡ��Ʋ�
B. �ŵ�ʱ�������ĵ缫��ӦʽΪ 3CO2��4Na����4e��===2Na2CO3��C
C. ԭ���缫������ȣ������ɵ�Na2CO3��Cȫ�������ڵ缫���棬��ת��0.2 mol e��ʱ��������������Ϊ11.2g
D. ѡ���{������-�ĸʴ������������Һ���ŵ��ǵ����Ժã�������Ʋ���Ӧ���ѻӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ���ܹ�ʹ��ѧ��Ӧ���ʼӿ���ǣ� ��
A.�����¶�
B.�����¶�
C.ʹ�ô���
D.������巴Ӧ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������ȼ�ϵ����һ�ָ�Ч����Ⱦ����������ּ�������KOH������ʣ������ԣ�������������ʣ�ȼ�ϵ�ء����������ȼ�ϵ������������Ӧ����ʽ��____________��
��2��������Ա��������ͼԭ���װ���������������ĵ缫��ӦʽΪ__________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ� ��
��31g�������1.5NA��P-P
��1L0.1 mol/L��Na2CO3��Һ�к�����������Ϊ0.1NA��
�۱�״���£�22.4 L HF��NA������
�ܵ�⾫��ͭʱת����NA�����ӣ������ܽ�32 gͭ
�ݱ�״���£�2.24 L Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA
���������£���0.2molH2SO4��Ũ����������ͭ��Ӧ������SO2�ķ�����С��0.1NA
��142gNa2SO4��Na2HPO4���������У���������������Ϊ3NA
��NA��Fe(OH)3�������ӵ�����Ϊ107g
A. �٢ۢܢ� B. �٢ޢ� C. �ۢݢ� D. �٢ޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ�ҩ������Ʒۡ�����غ�ľ̿��һ��������϶��ɵģ���ըʱ�ķ�Ӧ��S+2KNO3+3C=K2S+N2��+3CO2�����÷�Ӧ�Ļ�ԭ���ǣ� ��
A.CB.SC.KNO3D.S��KNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и��������У��ҳ����ʵ�������ڶ�Ӧ�Ŀո��ڣ�
��NO2��N2O4 ��12C��14C ��40 19K��40 20Ca
��������( )
)
��������( )
)
�� ��
�� ����ͱ���
����ͱ���
(1)��Ϊͬλ�ص���________��
(2)��Ϊͬ���칹�����________��
(3)��Ϊͬϵ�����________��
(4)Ϊͬһ�����ʵ���________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com