
【题目】下列粒子在水中能电离出大量氯离子的是( )
A.氯化钠
B.氯酸钾
C.氯化氢
D.氯化银
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
【题目】氮的化合物在生产、生活中广泛存在。
(1)键能是将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。已知下列化学键的键能如下表:

写出1mol气态肼(H2N-NH2)燃烧生成氮气和水蒸气的热化学方程式________________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s)![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:

①该反应为________(填“放热”或“吸热”)反应。
②乙容器在60min时达到平衡状态,则0~60min内用NO的浓度变化表示的平均反应速率v(NO)=____________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
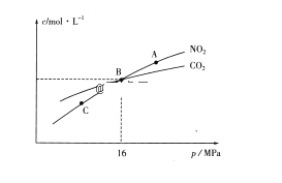
①A、C两点的浓度平衡常数关系:Kc(A)________Kc(C)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是________(填“A”或“B”或“C”)点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是:

①一定有乙烯 ②一定有甲烷 ③一定有丙烷 ④一定没有乙烷⑤可能有甲烷 ⑥可能有乙炔(C2H2)
A. ②④ B. ②③⑥ C. ②⑥ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宏观物质是由若干微粒构成的,微粒之间存在相互作用,下列说法错误的是( )。
A.NaCl是由Na+和Cl-通过离子键形成的离子晶体
B.SiO2和CO2均是原子晶体
C.含有共价键的化合物不一定是共价化合物
D.冰是水分子通过氢键和分子间作用力形成的分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
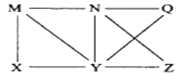
A. N一定是HCl(aq) B. X可能为Al或C12
C. Y一定为NaOH(aq) D. Q、Z中的一种必定为Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
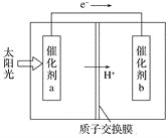
A. 该过程是将太阳能转化为化学能的过程
B. 催化剂a表面发生氧化反应
C. 催化剂a 附近酸性减弱
D. H+将在催化剂b的表面反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)取300 mL 0.2 mol/L的KI溶液与一定量的酸性 KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量为________________________。
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,又变为棕黄色的原因用离子方程式解释________________________________________。
(3)在1 L FeBr2溶液中通入标准状况下2.24 L Cl2,溶液中有1/4的 Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_________________。
(4)三氟化氮(NF3)是一种无色、无臭的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请写出该反应的化学方程式_________________________________________,反应中生成0.2 mol HNO3,转移的电子数目为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应的平衡常数表达式为K=![]() ,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是( )
,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是( )
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A. 该反应的化学方程式是CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B. 上述反应的正反应是放热反应
C. 若在1 L的密闭容器中通入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO为0.4 mol,则该反应达到平衡状态
D. 若平衡浓度符合下列关系式:![]() =
=![]() ,则此时的温度为1 000 ℃
,则此时的温度为1 000 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伪麻黄碱(I)是常见感冒药的成分之一,用于缓解感冒时带来的一些症状,其中一种合成路线如下:

已知:I.![]() (R、R'均代表烃基或氢原子)
(R、R'均代表烃基或氢原子)
II.A是衡量一个国家石油化工发展水平的重要标志之一;D的蒸气密度是相同条件下氢气密度的53倍。
回答下列问题:
(1)D的名称为_________________。F分子中最多有____________个原子在同一个平面上。
(2)I中含氧官能团的名称为_________________。H的结构简式为_________________。
(3)写出E在一定条件下与乙酸反应的化学方程式:_________________。
(4)G可以发生消去反应得到化合物M。写出M在一定条件下发生聚合反应的化学方程式:_________________。
(5)满足下列条件的E的同分异构体有____________种(不考虑立体异构)。
①属于苯的邻位二元取代物
②能与金属钠反应
(6)参照上述合成路线和相关信息,设计由A制备2-丁醇的合成路线(其他试剂任选):_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com