
【题目】有机物转化所需的试剂、反应条件中,不正确的是
A. 醇→烯烃:浓硫酸,加热
B. 醛→羧酸:银氨溶液,酸化,水浴加热
C. 苯→溴苯:溴水,铁
D. 酸→酯:醇,浓硫酸,加热
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值下列有关叙述正确的是
A. 常温常压下, 30 g乙烷中所含的极性共价键数为6NA
B. 0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA
C. 0.1 mol![]() Sr原子中含中子数为3.8NA
Sr原子中含中子数为3.8NA
D. 0.1mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既能与盐酸反应,又能与氢氧化钠溶液反应的化合物是( )
①Al(OH)3 ②Al2O3 ③Al ④NaHCO3 ⑤Mg(OH)2
A.①②③④B.①②③④⑤C.①②④D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细a-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程图如下:
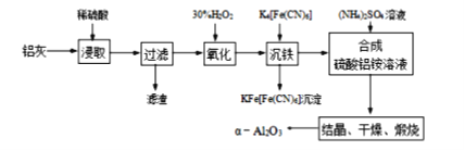
(1)铝灰中氧化铝与硫酸反应的化学方程式为_______。
(2)加30%的H2O2作用为将Fe2+氧化为Fe3+,其发生的离子反应方程式为__________。该反应需控制温度低于40℃,其目的是_____________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]=2Al2O3+2NH3↑+5SO3↑+3SO2↑+N2↑+53H2O,将产生的气体通过如图所示的装置。
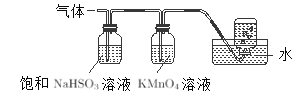
①足量饱和NaHSO3溶液吸收的物质除大部分H2O外还有________(填化学式)。集气瓶中收集到的气体是_______。
②KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程符合如图所示关系的是 ( )

A. 向Ba(NO3)2溶液中通入SO2气体至过量
B. 向Na2SiO3溶液中通入HCl气体至过量
C. 向澄清石灰水中通入SO2气体至过量
D. 向NaAlO2溶液中通入HCl气体至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是将Fe2+氧化为Fe3+ ,其离子方程式________________________,还可使用双氧水代替硝酸,其优点是_________________________________________。
(2)沉淀B的主要成分是_____、_______,往沉淀B中加入足量氢氧化钠溶液,现象是_________,该反应的离子方程式为____________________________________。
(3)加氨水过程需控制溶液的pH值,如何用pH试纸测定溶液的pH值___________。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:2![]() +6H++5H2C2O4=2Mn2++10CO2+8H2O。实验中称取0.800 g水泥样品,滴定时消耗了0.100 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________。
+6H++5H2C2O4=2Mn2++10CO2+8H2O。实验中称取0.800 g水泥样品,滴定时消耗了0.100 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A. 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B. 28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C. 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
D. 常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A. 该反应的化学方程式为3B+2D![]() 6A+4C
6A+4C
B. 反应进行到6s时,各物质的反应速率相等
C. 反应进行到6s时,B的平均反应速率为0.1mol/(Ls)
D. 反应进行到1s时,v(A)![]() 3v(D)
3v(D)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。下列说法正确的是( )
硫酸 化学纯 CP 500 mL
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84 g/cm3
质量分数:98%
A. 该硫酸的物质的量浓度为9.2 mol/L
B. 1 mol Fe与足量的该硫酸反应产生2 g氢气
C. 配制200 mL 4.6 mol/L的硫酸需取该硫酸50 mL
D. 等质量的水与该硫酸混合后所得溶液的物质的量浓度大于9.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com