
����Ŀ���F��һ�������HCl���壬��������l00mLϡ�����У�������Һ��������䣬������Һ�м���4mol/L��NaOH��Һl0mLǡ�ó����ԡ�����������������Һ�е��������Ba(OH)2��Һ�����ó�������Ϊ2.33g��
��1����������ʵ���Ũ�ȣ�__________mol/L
��2����HCl�����ڱ�״���µ����Ϊ__________mL.
��3������û�����Һ(��Ϊ100mL)�м���Na2CO3��10H2O���壬ֱ�����ٲ�������ʱΪֹ�� ����Na2CO3��10H2O���������Ϊ _________g��
���𰸡���0.lmol/L �� 488 �� 5.72
��������
�����������2��2.33gBaSO4�����ʵ���Ϊ��n=![]() =0.01mol������������غ�n(H2SO4)=n(BaSO4)=0.01mol��������������ʵ���Ũ��Ϊ0.01mol/0.1L=0.1mol/L��
=0.01mol������������غ�n(H2SO4)=n(BaSO4)=0.01mol��������������ʵ���Ũ��Ϊ0.01mol/0.1L=0.1mol/L��
��3�����ݷ���ʽH2SO4+2NaOH=Na2SO4 +2H2O��֪����0.01mol���ᷴӦ��Ҫ�������Ƶ����ʵ���Ϊ0.01mol��2=0.02mol���������ᷴӦ�������Ƶ����ʵ���Ϊ��0.01L��4mol/L-0.02mol=0.02mol���ɷ���ʽHCl+NaOH=NaCl+H2O��֪��n(HCl)=n(NaOH)=0.02mol��V=n �� Vm = 0.02 mol �� 22.4 mol/L = 0.448L=448mL��
��4��������Һ�м�������������Һ�������ķ�Ӧ��H2SO4+2NaOH=Na2SO4 +2H2O��HCl+NaOH=NaCl+H2O��ǡ�ó����ԣ�n(H+)=n(OH-)=0.04mol������Na2CO310H2O���壬������ӦCO32-+2H+�TCO2��+H2O��n(Na2CO310H2O)=n(CO32-)=1/2n(H+)=0.02mol������m(Na2CO310H2O)=nM=0.02mol��286g/mol=5.72g��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��
MgSO4(s)��CO(g)![]() MgO(s)��CO2(g)��SO2(g)��H��0
MgO(s)��CO2(g)��SO2(g)��H��0
�÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
ѡ�� | x | y |
A | �¶� | �����ڻ��������ܶ� |
B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
C | SO2��Ũ�� | ƽ�ⳣ��K |
D | MgSO4������(�������) | CO��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ�õ�����Ҫ����Դ��
(1)��25����101kPa�£�16g�ļ״�(CH3OH)��ȫȼ������CO2��Һ̬ˮʱ�ų�352kJ�����������ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ_____________________��
(2)��ѧ��Ӧ�зų�������(�ʱ䣬��H)�뷴Ӧ���������ļ���(E)�йأ�
��֪��H2(g)+Cl2(g)=2HCl(g)��H=��185kJ/mol��
E(H��H)=436kJ/mol��E(Cl��Cl)=243kJ/mol��E(H��Cl)=_____________
(3)����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע����֪��
2Cu(s)+![]() O2(g)�TCu2O(s)��H=��169kJmol��1��
O2(g)�TCu2O(s)��H=��169kJmol��1��
C(s)+![]() O2(g)�TCO(g)��H=��110.5kJmol��1��
O2(g)�TCO(g)��H=��110.5kJmol��1��
2Cu(s)+O2(g)�T2CuO(s)��H=��314kJmol��1
��ҵ����̿���ڸ��������»�ԭCuO��ȡCu2O��CO���Ȼ�ѧ����ʽ_____________��
(4)��ͼ��N2��H2��Ӧ����2molNH3�����������仯ʾ��ͼ��

�������ÿ����1molNH3�ų�����Ϊ��_________��
������ʼʱ�������ڷ���1molN2��3molH2��ƽ���N2��Ϊ20%����Ӧ�ų�������ΪQ1kJ����Q1����ֵΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦaA��g����bB��s��![]() cC��g���У����ʵĺ���A%��C%���¶��ı仯������ͼ��ʾ������˵����ȷ����
cC��g���У����ʵĺ���A%��C%���¶��ı仯������ͼ��ʾ������˵����ȷ����
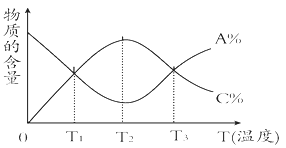
A���÷�Ӧ��T1��T3�¶�ʱ�ﵽ����ѧƽ��
B���÷�Ӧ���淴Ӧ�Ƿ��ȷ�Ӧ
C���÷�Ӧ��T2�¶�ʱ�ﵽ����ѧƽ��
D������������ƽ���������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����ȷ���� �� ��
A. Խ����ֲ����������ˮ����ˮ�ı�ֵ�½��������ڵֿ������Ļ�������
B. �����Ǵ����Ŵ���Ϣ�����Ƶ����ʺϳɵ���������
C. ���ۡ���ԭ����ά�غͺ��Ƕ�����������
D. ���ǡ������ʡ����������̼��Ϊ�Ǽܵ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼ����ؿ���������������Ĺ�����Դ��һ���ȼ����صĻ����ṹ��ͼ��ʾ����Ϊ����ʵ���ˮLiCl-KCl������������ں�ؼ���˲��������ܡ��õ���ܷ�ӦΪ��PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb�������й�˵����ȷ����

A��������Ӧʽ��Ca + 2Cl����2e�� = CaCl2
B���ŵ�����У�Li+���ƶ�
C������ʱ��������������ϵ�����������ƣ�ָ�뷢��ƫת
D��ÿת��0��1mol���ӣ�����������10��35 g Pb
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϸ���л��������ҪԪ��ռϸ�����صĺ������ɶൽ����ȷ�������ǣ� ��
A. ˮ�������ʡ�֬�ʡ����� O��C��H��N
B. ˮ�������ʡ����ࡢ֬�� C��O��H��N
C. ˮ�����ࡢ�����ʡ�֬�� O��C��H��N
D. ˮ��֬�ʡ������ʡ����� O��N��C��H
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���IL0.1mol/LNH4Cl��Һ�У����ϼ������NaOH��NH4+��NH3��H2O�ı仯��������ͼ��ʾ(����������仯�Ͱ��Ļӷ�)������˵������ȷ����

A��M����Һ��ˮ�ĵ���̶ȱ�ԭ��ҺС
B����M��ʱ��n(OH-)-n(H+)=(a-0.05)mol
C������NaOH�ļ��룬c(H+)/c(NH4+)��������
D����n(NaOH)=0.1molʱ��c(OH-)>c(Cl-)-c(NH3��H20)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҽ��������ˮ�IJ���ע����������Ϊ0.9%��NaCl��Һ������������ˮ��Ũ�ȸ��ߵ��Ȼ�����Һ��˵��
A. ��������������ϸ��
B. ˮ����������ϸ��
C. Na+��Cl���������ٶ��Ժ�ϸ���в�
D. ���ζ�ά��ϸ������̬��������Ҫ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com