
【题目】下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是
A. CaO + H2O = Ca(OH)2 B. 3NO2 + 2H2O = 2HNO3+NO
C. 2H2O![]() 2H2↑+O2↑D. 2Na +2H2O =2NaOH+H2↑
2H2↑+O2↑D. 2Na +2H2O =2NaOH+H2↑
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在10 mL浓度均为0.1 mol/L的AlCl3与MgCl2混合溶液中,加入60 mL、0.1 mol/L的NaOH溶液后,铝元素的存在形式是
A.Al3+、Al(OH)3B.Al(OH)3C.![]() lO2-、Al(OH)3D.
lO2-、Al(OH)3D.![]() lO2-
lO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:

(1)类比CO2的性质,学习SO2的性质,写出下列反应的离子方程式。
①少量的SO2通入澄清石灰水中:__________________。
②SO2通入Na2SO3溶液中: ________________________。
(2)Y的分子式:___________________。
(3)Z的稀溶液与铁反应的离子方程式为______________________。
(4)检验CO2是否混有SO2,可以使混合气体通过盛有品红溶液的洗气瓶,这是利用了SO2的_____________性,也可以使混合气体通过盛有酸性高锰酸钾稀溶液的洗气瓶,这是利用了SO2的_____________性。
(5)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原角度分析,合理的是__________(填字母选项)
A.Na2S+S B.Na2SO3+S C.Na2SO3+ Na2SO4 D.SO2+Na2SO4
(6)将X与SO2的水溶液混合后产生淡黄色沉淀,该反应的氧化产物与还原产物的质量之比为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
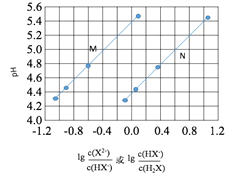
A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成。回答下列问题:

(1)B和A为同系物,B的结构简式为_______。
(2)反应①的化学方程式为___________,其反应类型为__________。
(3)反应③的反应类型为____________。
(4)C的结构简式为___________。
(5)反应②的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某待测溶液(阳离子为Na+)中只可能含有SO42-、SO32-、Cl-、Br-、NO3-、HCO3-中的一种或若干种,进行下列实验(每次实验所加试剂均足量):回答下列问题:
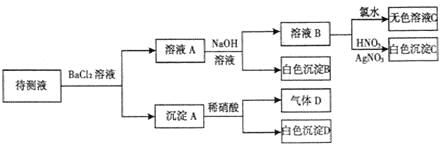
(1)待测液中是否含SO42-、SO32-离子__________________________________________
(2)气体D的化学式为____________,反应生成沉淀B的离子方程式为:____________
(3)根据以上实验,待测液中肯定没有的离子__________________________;肯定存在的离子是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
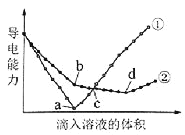
下列分析不正确的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH–
C.c点,两溶液中含有相同量的OH–
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO3![]() 4NO2↑+O2↑+2H2O)。
4NO2↑+O2↑+2H2O)。
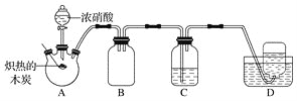
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至炽热状态,伸入三颈烧瓶中,生成的气体的颜色为__,产生该气体的反应的化学方程式是__。
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为__(填化学式)。
(3)装置B的作用是__。
(4)装置D中收集到了无色气体,有同学认为是NO,还有同学认为是O2。
①下列对该气体的检验方法合适的是__(填字母)。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶内收集到的无色气体是氧气,则氧气的来源是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色 气泡后,迅速停止 | Fe、Cu接触后,其表面 均产生红棕色气泡 |
下列说法中,不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否持续被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com