
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室利用SO2(g)和Cl2(g)合成硫酰氯的实验装置如下图所示(夹持装置已省略):

己知:①SO2(g)+Cl2(g)![]() SO2Cl2(I) ΔH=-97kJ/mol;
SO2Cl2(I) ΔH=-97kJ/mol;
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气
回答下列问题:
(1)装置H的名称是_______________,装置E中活性炭的作用是 _____________。
(2)请指出下列装置中应盛入的试剂:B_____________、F________________。
(3)若采用实验室制法制取Cl2,其发生装置应选择_________装置 (用A、B、C等编号填空〉,其中发生反应的离子方程式为____________________。
(4)为什么硫酰氯在潮湿空气中易“发烟”____________ (结合化学方程式说明)。
(5)为了使通入反应器的SO2和Cl2达到最佳反应比例,可观察_________(填现象)来反映通入气体的速率,利用反应液的滴加快慢对气体通入速率加以控制。
(6)该装置尚存在明显的缺陷,请指出_____________________。
【答案】 冷凝管 利用活性炭对气体的吸附作用,提供反应载体 饱和食盐水 浓硫酸 A MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O SO2Cl2 +2H2O === H2SO4+2HCl,HCl结合水蒸汽形成白雾 装置C和F中产生气泡的快慢 末端没有尾气处理装置和干燥装置,污染大、外界水蒸汽易进行装置内
Mn2++Cl2↑+2H2O SO2Cl2 +2H2O === H2SO4+2HCl,HCl结合水蒸汽形成白雾 装置C和F中产生气泡的快慢 末端没有尾气处理装置和干燥装置,污染大、外界水蒸汽易进行装置内
【解析】根据装置图可知,装置A用于提供氯气,B、C为除杂装置,G为生成二氧化硫的装置,硫酰氯易水解,因此氯气与二氧化硫需干燥,干燥氯气与二氧化硫的反应需要用活性碳作催化剂,硫酰氯易水解易挥发,所以在三颈烧瓶上方应连接一个冷凝管和装有碱石灰的干燥管。
(1)根据装置图,装置H是冷凝管,装置E中活性炭具有吸附性,可以提供反应的载体,作催化剂,故答案为:冷凝管 (2). 利用活性炭对气体的吸附作用,提供反应载体(或催化剂);
(2) B、C为除去氯气中的氯化氢和水蒸气,因此B装置中应该盛放饱和食盐水,C中盛放浓硫酸,F为干燥二氧化硫的装置,可以选用浓硫酸,故答案为:饱和食盐水;浓硫酸;
(3)根据上述分析,若采用实验室制法制取Cl2,其发生装置应选择A装置,其中发生反应的离子方程式为MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O,故答案为:A;MnO2+2Cl-+4H+
Mn2++Cl2↑+2H2O,故答案为:A;MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(4) SO2Cl2 +2H2O = H2SO4+2HCl,HCl结合水蒸汽形成白雾,造成硫酰氯在潮湿空气中易“发烟”,故答案为:SO2Cl2 +2H2O = H2SO4+2HCl,HCl结合水蒸汽形成白雾;
(5)为了使通入反应器的SO2和Cl2达到最佳反应比例,可观察装置C和F中产生气泡的快慢来反映通入气体的速率,故答案为:装置C和F中产生气泡的快慢;
(6)氯气和二氧化硫均能够污染空气,该装置中末端没有尾气处理装置和干燥装置,污染大、外界水蒸汽也易进行装置E内,故答案为:末端没有尾气处理装置和干燥装置,污染大、外界水蒸汽易进行装置内。


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验的说法正确的是( )
A. 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B. 将钠投入到盛满水的烧杯中,观察钠与水反应实验现象
C. 制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D. 实验室配制一定浓度NaOH溶液,将称量固体溶解后马上转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素在生活中有广泛应用,根据所需知识回答下列问题。
(1)氟元素基态原子的价电子排布图:_________,卤族元素位于元素周期表______区。
(2)在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______________。
(3)BF3常温下是气体,有强烈的接受弧电子对的倾向。BF3分子的立体构型为______,固态时的晶体类型是_______,BF3与NH3相遇立即生成白色固体,写出该白色固体物质的结构式并标注出其中的配位键_____。
(4)根据下表提供的数据判断,熔点最高、硬度最大的是_______(填化学式)。
离子晶体 | NaF | MgF2 | AlF3 |
晶格能(KJ·mol-1) | 923 | 2957 | 5492 |
(5)已知NaClO2晶体中阴离子为V型,ClO2-中氯原子的弧电子对数是______,ClO2-中氯原子的杂化轨道类型为_____,HClO4比HClO2酸性强的原因是_______。
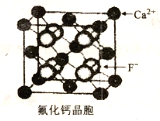
(6)CaF2晶胞如下图所示。已知:NA为阿伏伽德罗常数,棱上相邻的两个Ca2+的核间距为acm,则CaF2的密度可表示为_____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以菱镁矿(主要成分为MgCO3、含少量FeCO3、SiO2)制备高纯氧化镁的流程如下图所示:

己知:25℃时,指示剂变色pH范围和几种氢氧化物的ksp及pH的关系如下表:
指示剂 | 酚酞 | 甲基酸 |
变色范围(pH) | 8.2-10.0 | 3.1-4.4 |
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀时pH | 1.1 | 5.9 | 8.4 |
沉淀完全时pH | 3.7 | 9.6 | 10.2 |
溶度积常数 | 4×10-34 | 8×10-16 | 2×10-13 |
(1)操作II和III中涉及的分离方法分别是____________、_______________。
(2)残渣I的主要成分是____________,加入H2O2的过程中可观察到的现象是___________,其中发生的离子反应方程式是_________________________。
(3)MgSO4和木炭在800℃煅烧时,只生成MgO和两种气体,将混合气体通入NaOH溶液时,气体被完全吸收。煅烧时发生反应的化学方程式是_____________。
(4)采用滴定法测定溶液II与加入氨水的最佳体积比,可以减少氨水的消粍和Mg2+的损失。实验中应选取_______________指示剂,加入氨水是为了沉淀溶液II中的___________离子,若终点时该离子浓度=1.0×10-5mol·L-1,则溶液III的pH=_____________(己知:lg2=0.3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空:
(1)写出氯化钠的电子式_______________,氮气的结构式______________;
(2)用离子方程式表示氨水溶液显碱性的原因_________________;
用离子方程式表示碳酸钠溶液显碱性的原因_____________________;
(3)某碳氢化合物的相对分子质量为72,且一个分子结构中有3个甲基,则该有机物的结构简式为____________,该有机物的系统命名是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol·L-1CH3COONa溶液pH =a,则下列说法正确的是
A.CH3COOH在常温下Ka数值约为l×101-2a
B.约有1.0×l0a-14 mol·L-1的水发生电离
C.加热后溶液pH <a
D.加少量水后,溶液pH >a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列物质中,不属于芳香族化合物的是_______,属于芳香烃的是________,属于苯的同系物的是___________。(填编号)

II.己知某有机物的相对分子质量为58。根据下列条件回答:
若该有机物的组成只有C、H,则此有机物的分子式为______________;若它的核磁共振氢谱只有2个峰,则它的结构简式为______________,__________________。
III.有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃。下 图中椭圆烯也属于稠环芳香烃。据此回答:

(1)己知椭圆烯(I)的分子式为C24H12,则椭圆烯(II)的分子式为_______________;
(2)上述椭圆烯的一氯取代物各有几种同分异构体:(I)有_______种,(II)有_______种;
(3)假设上述椭圆烯可以和氢气在一定条件下发生加成反应生成饱和脂环烃,则加氢后的
生成物分子中所有的碳原子是否在同一平面内:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是氮元素在煤粉使用过程中的转化关系:

(1)③中加入的物质可以是___________(填标号)。
a.空气b.CO c.KNO3d.NH3
已知:N2(g) +O2(g)=2NO(g) △H = a kJ·mol-1
N2(g)+3H2(g)=2NH3(g) △H = b kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H = c kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H = d kJ·mol-1
上面转化关系反应后恢复至常温常压,根据以上信息写出③中你所选物质参与反应的热化学方程
式___________(如果所选物质不只一种,则只要写出其中一个热化学方程式即可)。
(2)将烟气中的氮氧化物(NOx)转化为无害物质,这个过程称为脱硝。下面反应为处理方法之一:
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
①若反应生成1molN2,则反应中转移的电子数为___________mol。
②使上述反应速率增大且平衡向右移动的措施是___________。
③氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如图所示,则X是___________(填化学式)。在体积为2L的容器中模拟进行上述反应,初始时加入8molNO和3.5molO2,氨氮比为0.5时,该反应的平衡常数K =___________(保留二位小数)。当n(NH3)/n(NO)>1.0 时,烟气中NO浓度反而增大,主要原因是___________(用化学方程式表示)。

④若上述反应在与外界绝热的容器中进行,氨氮比由0.5增加到1.0时,在此过程中该反应的平衡常数___________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com