
【题目】下列实验操作不是从安全角度考虑的是
A.用氯酸钾和二氧化锰制氧气时用排水法收集后,应从水中撤出导管后再停止加热
B.酒精灯在不使用时,必须盖上灯帽
C.实验室制备CO气体必须在通风橱中进行
D.蒸馏操作时应在混合液中加入沸石
科目:高中化学 来源: 题型:
【题目】五种短周期主族元素W、M、X、X、Z原子序数依次增大,请结合表中信息回答下列问题:
元素 | W | M | X | Y | Z |
结构或性质 | 最高价含氧酸与其气态氢化物能发生化合反应 | 氢化物的水溶液能刻蚀玻璃 | 焰色反应呈火焰黄色 | 同周期主族元素形成的简单离子中,其离子半径最小 | 最高正价与最低负价代数和为6 |
(1)M元素在周期表中的位置为____________。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为__________(用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为_____。
(4)下列可作为比较M和Z的非金属性强弱的依据是_______(填序号)。
A.单质与H2反应的难易程度 B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱 D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)常温下,4.6gX单质在空中燃烧,再恢复到常温,放出QkJ能量,该反应的热化学方程式为_______________。
(6)W能形成多种氢化物,其中-种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式___________。该氢化物和O2在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式____________。
(7)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧a g乙醇(液态),生成二氧化碳气体和液态水,放出的热量为Q kJ,经测定,a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,则表示乙醇燃烧热的热化学方程式书写正确的是( )
A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H = -Q kJ/mol
B.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H = - Q / 2 kJ/mol
C.![]() C2H5OH(l)+
C2H5OH(l)+ ![]() O2(g)=CO2(g)+3/2H2O(l) △H = -Q kJ/mol
O2(g)=CO2(g)+3/2H2O(l) △H = -Q kJ/mol
D.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H = -2Q kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.胶体与溶液的本质区别在于是否具有丁达尔效应
B.电解质电离需要通电才能实现
C.只含有一种元素的物质一定是纯净物
D.向Fe(OH)3胶体中逐滴滴加稀硫酸,先出现沉淀,后来沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释
B. 反应2CO+2NO = N2+2CO2在常温下能自发进行,则反应的![]() H>0,
H>0,![]() S<0
S<0
C. 0.1mol·L-1NH4Cl溶液加水稀释,c(H+)/c(NH4+)的值增大
D. 反应CH3COOCH3+H2O![]() CH3COOH+CH3OH
CH3COOH+CH3OH ![]() H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大
H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) = 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) = C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) = 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2 (g) = 2H2O(l) ΔH=-d kJ·mol-1 (abcd均为正值)
请回答下列问题:
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量(填“大于”、“等于”或“小于”)途径II放出的热量。
②b 与a、c、d的数学关系式是 。
(2)甲醇是一种重要的试剂,有着广泛的用途,工业上可利用CO2制备甲醇。用CH4与CO2反应制H2和CO,再利用H2和CO化合制甲醇。已知:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H1=-1450.0kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
③ 2H2(g)+O2(g)=2H2O(l) △H3=-571.6kJ·mol-1
则H2和CO制液态甲醇的热化学方程式为。
(3)如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.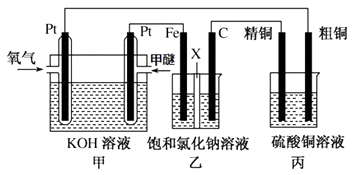
报据要求回答相关问题:
①写出甲中通甲醚一极的电极反应式。
②乙中发生的总反应的离子方程式为。
③将0.2mol AgNO3、0.4mol Cu(NO3)2 、0.6mol KCl溶于水,配成100ml溶液,用惰性电极电解一段时间后,某一电极上析出了0.3mol Cu,此时在另一电极上产生的气体体积(标准状况)为 L,若要使电解质溶液恢复到电解前的状态,需要加入固体的质量为g 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 | Ka1=5.9×10-2 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为。
(2)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为。
(4)若0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=mol·L-1(填精确计算结果)。
(5)将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L 1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度由大到小的顺序为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物貭的量之向的关系如图所示。则下列説法正确的是( )

A. 溶液中的阳离子一定含有H+、Mg2+、Al3+,可能含有Fe3+
B. 溶液中一定不含CO32-和NO3-,一定含有SO42-
C. 溶液中C(NH4+)=0.2mol/L
D. c(H+):c(Al3+):c(Mg2+)=l:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性.纳米泡沫碳与金刚石的关系是( )
A.同一种物质
B.同分异构体
C.同位素
D.同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com