
【题目】可检查淀粉部分发生水解的试剂是( )
A.碘水B.碘化钾溶液
C.硝酸银溶液D.银氨溶液、碘水
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到相应目的的是( )
A | B | C | D | |
实验装置 |
|
|
|
|
目的 | 验证Fe与稀盐酸反应放热 | 测定中和热 | 制备干燥的NH3 | 分离I2和NH4Cl |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3溶液与盐酸反应过程中的能量变化示意图如图,下列反应属于吸热反应的是( )
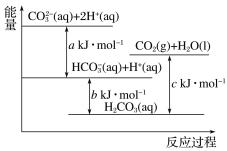
A. CO32-(aq)+H+(aq)=HCO3-(aq)
B. CO32-(aq)+2H+(aq)=CO2(g)+H2O(l)
C. HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)
D. CO2(g)+H2O(l)=H2CO3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛。
(1)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是____(填序号)。
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(2)碘元素可预防甲状腺肿大,因此我国市场上的食盐均加了碘(KIO3)。甲同学鉴别食盐是否加碘的流程如下:
![]()
①若样品为加碘食盐,则现象应为_____,此方法中KI的作用是_____。
②乙同学取纯NaCl作样品做对照实验,也出现了明显的现象,原因是____。
③丙同学提出新的鉴别加碘食盐的方案,流程如下:
![]()
此方案第一步涉及反应的离子方程式为____。
(3)已知反应2HBr(g) = H2(g) + Br2(g) ΔH= +102 kJ·mol-1。
①1molH2(g)、1molBr2(g)分子中化学键断裂时分别需要吸收436kJ、200kJ的能量,则1molHBr(g)分子中化学键断裂时需吸收的能量为___kJ。
②某温度下,向体积为2L的密闭容器中通入amol HBr气体,10min后测得Br2蒸气的浓度为bmol/L,则此段时间内υ(HBr)=____。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。

B→A+C反应的热化学方程式为____(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l) ΔH =-285.8 kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH =-241.8 kJ/mol
③C(s)+1/2O2(g)=CO(g) ΔH =-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ/mol
回答下列问题:
(1)H2的燃烧热ΔH=_______;C的燃烧热为__________。
(2)燃烧1 g H2生成液态水,放出的热量为_________。
(3)已知CO的燃烧热为283.0 kJ/mol,现有CO、H2和CO2组成的混合气体116.8 L(标准状况),完全燃烧后放出总热量为867.9 kJ,且生成18 g液态水,则混合气体中H2为_________L,CO在混合气体中的体积分数约为_________(精确至小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.用水分离四氯化碳和酒精的混合物
B.蒸馏完毕时,先再停止加热,关闭冷凝水
C.配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸 馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释
D.将放在称量纸上称取的NaOH固体在烧杯中溶解,待冷却后,再转移至容量瓶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com