
����Ŀ����������������Ⱦ���Ż������ʾ�������Ҫ��
��1����CH4����ԭ�����������������������Ⱦ�����ķ�Ӧ���£�
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ��H=-574kJ/mol
4NO(g)+CO2(g)+2H2O(g) ��H=-574kJ/mol
CH4(g)+4NO2(g)![]() 2N2(g)+CO2(g)+2H2O(g) ��H=-1160kJ/mol
2N2(g)+CO2(g)+2H2O(g) ��H=-1160kJ/mol
����0.2molCH4��NO2��ԭΪN2�������������зų�������Ϊ________kJ��������ˮȫ������̬��ʽ���ڣ�
��2���û���̿�ɴ���������Ⱦ��NO����2L�ܱ������м���NO�ͻ���̿�������ʣ�����������E��F�����ڶȷֱ���T1��T2ʱ����÷�Ӧ�ﵽƽ��ʱ���������ʵ������±���

�������ϱ����ݣ�д��NO�����̿��Ӧ�Ļ�ѧ����ʽ_______________��
��T1�� ʱ��������Ӧ��ƽ�ⳣ����ֵΪ________�������֪T2��T1����÷�Ӧ����Ӧ�ġ�H___���>����<����=����0
�� ��T1�¶��·�Ӧ�ﵽƽ������д�ʩ��������NOת���ʵ���_______��
a�������¶� b������ѹǿ c.����c(NO) d����ȥ����F
��3������β�������еķ�Ӧ��2NO+2CO![]() 2CO2+N2��ij�¶�ʱ����1L�ܱ������г���0.1molCO��0.1mol NO��5sʱ��Ӧ�ﵽƽ�⣬���NO��Ũ��Ϊ0.02mol/L����Ӧ��ʼ��ƽ��ʱ��NO��ƽ����Ӧ����v(NO)=________�������¶��£�ijʱ�̲��CO��NO��N2��CO2��Ũ�ȷֱ�Ϊ0.01mol/L��amol/L��0.01mol/L��0.04mol/L��Ҫʹ��Ӧ������Ӧ������У�a��ȡֵ��ΧΪ_____________��
2CO2+N2��ij�¶�ʱ����1L�ܱ������г���0.1molCO��0.1mol NO��5sʱ��Ӧ�ﵽƽ�⣬���NO��Ũ��Ϊ0.02mol/L����Ӧ��ʼ��ƽ��ʱ��NO��ƽ����Ӧ����v(NO)=________�������¶��£�ijʱ�̲��CO��NO��N2��CO2��Ũ�ȷֱ�Ϊ0.01mol/L��amol/L��0.01mol/L��0.04mol/L��Ҫʹ��Ӧ������Ӧ������У�a��ȡֵ��ΧΪ_____________��
��4��ij������������ͼ��ʾװ�ã�̽��NO2��O2��������N2O5�γ�ԭ��صĹ��̡�����Y������Ϊ_______���õ�ص�������ӦʽӦΪ___________��

���𰸡� 173.4 C+2NO![]() N2+CO2 0.5625 < bc 0.016mol/(L��s) a>0.01 ���������� O2+2N2O5+4e-=4NO3-
N2+CO2 0.5625 < bc 0.016mol/(L��s) a>0.01 ���������� O2+2N2O5+4e-=4NO3-
����������1����֪��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ��mol��1����CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1 160kJ��mol��1�����ø�˹���ɽ�(��+��)/2���ɵ�CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g������H=-��574+1160��/2kJ��mol��1=867kJ��mol��1��n��CH4��=4.48L/22.4L��mol��1=0.2mol�����������зų�������Ϊ0.2mol��867kJ��mol��1=173.4kJ��
�ʴ�Ϊ��173.4��
(2)���ɱ������ݿ�֪��T1ʱC��NO��E��F�Ļ�ѧ������֮��Ϊ0.03��0.06��0.03��0.03=1��2��1��1����Ӧ��C�����������ԭ���غ��֪������ΪN2��CO2���Ҹ÷�ӦΪ���淴Ӧ���ʷ�Ӧ����ʽΪ��C+2NO![]() N2+CO2��
N2+CO2��
�ڴӱ������ݿ�֪T1��ʱ��ƽ��Ũ��c��NO��=0.04mol/1L=0.04mol��L��1��c��N2��=c��CO2��=0.03mol/1L=0.03mol��L��1����T1��ʱ�÷�Ӧ��ƽ�ⳣ��ΪK1=0.03��0.03/0.042=9/16= 0.5625���ʴ�Ϊ�� 0.5625
�ɱ������ݿ�֪���¶���T1��ΪT2��ƽ�����淴Ӧ�ƶ���T2��T1����÷�Ӧ����Ӧ�ġ�H<0��
�� ���������ӦC+2NO = N2+CO2 ,��T1�¶��·�Ӧ�ﵽƽ�����a����Ϊ����Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���NOת�������� b���ڷ�Ӧǰ������������䣨������������2=1+1��������ѹǿ ��ƽ�ⲻ�ƶ���NO��ת���ʲ��䣻C�� c.����c(NO) ��C�ǹ��壬���ڷ�Ӧǰ������������䣨������������2=1+1������ʵ����һ����Чƽ�⣬�ں��º�ѹ�������������ȵ�������,ֻҪ�ǰ���ʼʱ���뷴Ӧ��ı������뷴Ӧ�����ƽ�������֮ǰ��ƽ���ǵ�Ч�ģ�Ҳ���Ǹ������������ٷֱ���ͬ�����ʵ����İٷ�������������ٷ�����ȣ���NO��ת���ʲ��䣻 d����ȥ����F ���൱�ڼ�С������Ũ�ȣ�ƽ�������ƶ���NOת��������bc�������⣬ѡbc��
��3�� 2NO + 2CO![]() 2CO2 + N2
2CO2 + N2
��ʼ/mol��L��1 0.1 0.1 0 0
��Ӧ/mol��L��1 0.08 0.08 0.08 0.04
ƽ��/mol��L��1 0.02 0.02 0.08 0.04
v(NO)=0.08mol��L��1/5s=0.016mol/(L��s)
T1��ʱ����1L���ܱ������У�����0.1mol CO��0.1mol NO���ﵽƽ��ʱ�����NO��Ũ��Ϊ0.02mol��L-1������¶���ƽ�ⳣ��K=![]()
ijʱ�̲��CO��NO��N2��CO2��Ũ�ȷֱ�Ϊ0.01mol��L��1��a mol��L��1��0.01mol��L��1��0.04mol��L��1��Ҫʹ��Ӧ�����������Q��K=1600
Q=![]() ��a��0.01��
��a��0.01��
��4��ʯīI�ǵ�ظ�����NO2ʧȥ���ӣ������ϼ����ߣ�YΪN2O5������Ϊ�������������������������ԭ��Ӧ���缫��ӦΪ�� O2+2N2O5+4e-=4NO3-��


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���ijFeCl2��Һ�Ƿ���ʣ���ѡ�õ��Լ��ǣ� ��
A. K3[Fe(CN)6]��Һ B. ʯ����Һ C. KSCN��Һ D. ����KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�м�������NaHSO4�����¶Ȳ���ʱ����Һ�� ( )
A��c(H��)/c(OH��)���� B��c(H��)��С
C��ˮ��c(H��)��c(OH��)�ij˻����� D��c(OH��)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������ڵ���ʵ��ǣ� ��
��NaOH��BaSO4��Cu�����Ǣ�CO2 ��
A.�٢�
B.�٢ڢ�
C.�ۢ�
D.�٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������绷�����˵�Ҫ����������ClO2����ȡ��Cl2��Ϊ����ˮ������������ҵ��ClO2����NaClO3��Na2SO3��Һ��ϲ���H2SO4�ữ��Ӧ�Ƶã���Ӧ��Na2SO3ת��Ϊ
A. SO2 B. Na2SO4 C. S D. Na2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ� ��
A. ��������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA
B. 0.5molO3��11.2LO2�����ķ�����һ�����
C. ���ʵ���Ũ��Ϊ0.5mol/L MgCl2��Һ������Cl����ΪNA
D. 1molFe������ϡ���ᷴӦʱ��ת�Ƶ��ӵ���ĿΪ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д��ȷ���� ( )
A��������ͭ��Һ�м����������������ҺBa2����SO![]() ��BaSO4��
��BaSO4��
B������ˮ�ķ�ӦNa+2H2O=Na++2OH-+H2��
C������ͨ������������Һ��2Cl2��2OH����3Cl����ClO����H2O
D������ʯ���ڴ���ķ�ӦCaCO3+2CH3COOH=Ca2++2CH3COO-+CO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. Ϊ�Ƚ�Cl2��Fe3+��SO2�������ԣ�����ͼ��ʾװ�ý���ʵ�飬��������£�

��.���ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�͵��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��
��.����a���μ�һ������Ũ���ᣬ��A���ȡ�
��.��B�е���Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��.����b��ʹԼ2mL����Һ����D�Թ��У��������е����ӡ�
��.���ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
��.�����Թ�D���ظ����̢ܣ�����B��Һ�е����ӡ�
��1�����н������ҺΪ__________��
��2����A�������������36.5%�ܶ�Ϊ1.2g/mL����100mLʱ���䷴Ӧת�Ƶĵ�����ĿΪ______��
��3�����̢��м���B��Һ���Ƿ�����������ӵIJ�����___________��
��4���ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤�������Ե���____ͬѧ����������˳��Ϊ____________��
���̢� B��Һ�к��е����� | ���̢� B��Һ �к��е����� | |
�� | ��Fe3+��Fe2+ | ��SO42�� |
�� | ����Fe3+����Fe2+ | ��SO42�� |
�� | ��Fe3+��Fe2+ | ��Fe2+ |
II. NaNO2����Ҫ�ķ�������+3�۵ĵ�����������Ӧ�������Ի����в��ȶ�����5mol/Lˮ��ҺpHΪ9��ij��ѧ��ȤС���������ͼ��ʾװ���Ʊ��������ơ�������Ǣٹرյ��ɼУ���A�з�Һ©���������μ�һ����Ũ���ᣬ���ȣ���һ��ʱ���ֹͣ���ȡ��ش��������⣺

��1��B�й۲����Ҫ������__________��Dװ�õ�������____________��
��2������C�в������������ƵIJ�����_______����Ӧ��Ӧ����ʽΪ___________��
��3��������C�в����������ƺ������١�a. ��ͬѧ��ΪC�в��ﲻ�����������ƣ������������ʡ�Ϊ�ų����ţ�����B��Cװ�ü�����װ��E��E��ʢ�ŵ��Լ���_______��д���ƣ���b. ��ͬѧ��Ϊ���������������⣬�������������뷴Ӧ���²�Ʒ������������ʵ�������ǰӦ����һ���������ò�����___��
��4���������������HNO2��Ka��ֵΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ��������з�Ӧ�ϳɼ״�CO��g��+2H2��g��CH3OH��g����H
��1���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶� | 250�� | 300�� | 350�� |
K | 3.041 | 1.000 | 0.120 |
�ɱ��������жϡ�H 0�����������=������������ѧƽ�ⳣ������ʽK= ��
��2��300��ʱ�������Ϊ2.0L���ܱ�������ͨ��2mol CO��4mol H2������20s �ﵽƽ��״̬��
�ټ���20s��CO�ķ�Ӧ����Ϊ ����ʱ�����м״����������Ϊ ��
����������ƽ����ϵ��ͬʱ����1mol CO��2mol H2��1mol CH3OH���壬ƽ���ƶ������
������ҡ����������ƶ�������ԭ���� ��
��3����֪�ڳ��³�ѹ�£�
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1=��1277.0kJ/mol
��2CO��g��+O2��g��=2CO2��g����H2=��566.0kJ/mol
��H2O��g��=H2O��l����H3=��44kJ/molд���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��4���״�������������ȼ�ϵ�أ�д������������Ϊ����ʼ״�ȼ�ϵ�ظ�����Ӧʽ ����ͼ�����KI��Һ�Ƶ⣬�ڴ��Թ��м��뱥�͵�KI��Һ��Ȼ���ټ��뱽������һ��ʯī�缫��һ�����缫��ʹ�ø�ȼ�ϵ������Դ�����缫�� ���������������ӣ�ͨ��һ��ʱ��Ͽ���Դ�����Թܣ��ϲ���ҺΪ ɫ������1.27g �ⵥ������ʱ����Ҫ g CH3OH��
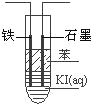
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com