
| A. | 道尔顿 | B. | 卢瑟福 | C. | 玻尔 | D. | 爱因斯坦 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 制取 聚苯乙烯
制取 聚苯乙烯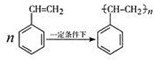
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一定条件下的电离程度 | B. | 属于离子化合物还是共价化合物 | ||
| C. | 熔融状态下是否完全电离 | D. | 溶于水后的导电能力是强还是弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题:
2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.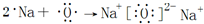 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低 | |
| B. | 将铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性 | |
| C. | 向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动 | |
| D. | 向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 标号 | HX | YOH | 溶液的体积关系 |
| ① | 强酸 | 强碱 | V(HX)=V(YOH) |
| ② | 强酸 | 强碱 | V(HX)<V(YOH) |
| ③ | 弱酸 | 弱碱 | V(HX)=V(YOH) |
| ④ | 弱酸 | 强碱 | V(HX)=V(YOH) |
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
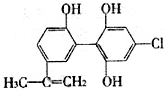 在2010年温哥华冬奥会上,有个别运动员因服用兴奋剂被取消参赛资格.如图是某兴奋剂X的结构简式,下列有关说法正确的是( )
在2010年温哥华冬奥会上,有个别运动员因服用兴奋剂被取消参赛资格.如图是某兴奋剂X的结构简式,下列有关说法正确的是( )| A. | 1molX在一定条件下与足量的氢气反应,最多消耗1molH2 | |
| B. | 1molX与足量的Na反应,最多产生标况下33.6LH2 | |
| C. | 1molX与足量的浓溴水反应,最多消耗5molBr2 | |
| D. | 1molX与足量的NaOH溶液在一定条件下反应,最多消耗5molNaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com