
| A. | 冰的密度比液态水的密度小 | B. | NH3易液化 | ||
| C. | NH3比PH3分子稳定 | D. | 乙醇以任意比例溶于水 |
分析 氢键的存在,影响到物质的某些性质.如熔点、沸点,溶解度,粘度,密度.
解答 解:A、冰和水的密度不同主要是由于水分子间存在氢键,氢键在水液态是使一个水分子与4个水分子相连,而当水凝固时氢键会拉伸水分子 使水分子之间距离增大 体积也就增大了,密度也就小了,故A正确;
B、氨气内部存在氢键(分子间的一种作用力),使得其熔沸点升高,所以氨气容易液化,故B正确;
C、由于N的非金属性大于P,所以NH3分子比PH3分子稳定,故C错误;
D、乙醇与水分子间存在氢键,所以乙醇以任意比例溶于水,故D正确;
故选:C.
点评 本题需要注意的是氢键的存在,影响到物质的熔点、沸点,溶解度,粘度,密度.而非金属性强弱只影响分子的稳定性,不影响沸点.


科目:高中化学 来源: 题型:选择题
| A. | 碳-12的原子符号:12 6C | |
| B. | 次氯酸分子的结构式:H-O-Cl | |
| C. | 硫离子的电子排布式为:1s22s22p63s23p6 | |
| D. | 二氧化硅的分子式:SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
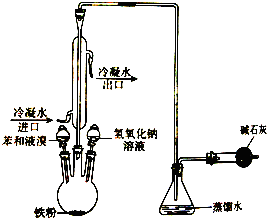 如图是实验室制取溴苯的装置图,请回答下列问题:
如图是实验室制取溴苯的装置图,请回答下列问题:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: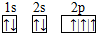 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,该化合物属于离子化合物(填“共价”或“离子”).
,该化合物属于离子化合物(填“共价”或“离子”). ,该化合物含的化学键类型是共价键.
,该化合物含的化学键类型是共价键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com