
【题目】某学生的实验报告中,描述合理的是
A. 用托盘天平称量25.20g NaCl
B. 用pH试纸测得NaClO溶液的pH约为11
C. 用25mL碱式滴定管量取出15.00mLKMnO4溶液
D. 将CuSO4溶液蒸发浓缩、降温结晶、过滤得到硫酸铜晶体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 铁跟稀硫酸反应:2Fe + 6H+ ===2Fe3+ + 3H2 ↑
B. 盐酸与澄清石灰水反应:H+ + OH===H2O
C. 氯化铝溶液与过量氨水反应:Al3++3OH-=Al(OH)3↓
D. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH===![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙可以作为生氢剂(其中CaH2中氢元素为﹣1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是( )
A.既不是氧化剂也不是还原剂
B.是氧化剂
C.是还原剂
D.既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.15mol/L,c(Cl﹣)=0.2mol/L,则c(NO3﹣)为( )
A.0.05 mol/L
B.0.20 mol/L
C.0.30 mol/L
D.0.40 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的恒温恒容密闭容器中发生反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L。则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L。则下列判断正确的是
A. c1:c2=1:2 B. 平衡时,Y和Z的生成速率之比为2:3
C. 若反应正向进行,X、Y的转化率不相等 D. c1的取值范围为0<c1<0.14mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铜、氯化亚铜是重要的化工原料,广泛用作有机合成的催化剂。
Ⅰ.实验室用右图所示装置,利用还原铜粉和氯气来制备氧化铜。
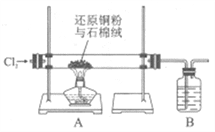
(1)石棉绒的作用是_______________。
(2)装置B中的试剂是_______________。
(3)所得产品中CuCl2的质量分数为90%,则其中可能含有的杂质是_______________(写一种即可)。
Ⅱ.另取纯净CuCl2固体用于制备CuCl。
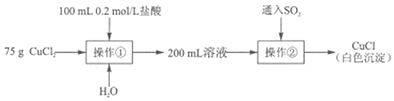
(4)操作①中加入盐酸的目的主要是_______________。
(5)操作②中反应的离子方程式为_______________。
(6)操作①中若用10mol/L盐酸代替0.2mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。
为验证此猜想,取75gCuCl2固体、100mL0.2mol/L盐酸及_______________mL9.8mol/LH2SO4配制成200mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:c(Cl-)过大导致白色沉淀溶解。
[资料显示:存在平衡2Cl-(aq)+CuCl(s)![]() CuCl32-(aq)]
CuCl32-(aq)]
请设计实验说明该猜想是否成立:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁矿石(若只含铁的氧化物和SiO2)取36g溶于过量的稀盐酸中,过滤、洗涤、干燥后得5.6g不溶物,向得到的滤液中加入足量的NaOH溶液,过滤、洗涤后将沉淀灼烧,得32g红棕色固体.根据题意下列结论不正确的是( )
A. 由铁矿石转化为红棕色固体的过程中发生了氧化还原反应
B. 溶于盐酸后得到的滤液中n(Fe2+):n(Fe3+)=1:1
C. 铁矿石中的铁的氧化物的化学式一定是Fe3O4
D. 若稀盐酸为3.0molL﹣1 400mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是0.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,1体积X2(气)和3体积Y2(气)化合成2体积的气体化合物,则该气体化合物的化合式为( )
A.XY3
B.XY
C.X3Y
D.X2Y3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com