
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)。下列推断不正确的是( )
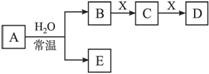
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+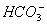 ====H2O+
====H2O+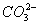 ,则E一定能还原Fe2O3
,则E一定能还原Fe2O3
C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是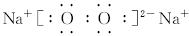
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:
8 有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
A. X、M两种元素只能形成X2M型化合物
B. 由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次 降低
降低
C. 元素Y、Z、W的单质晶体属于同种类型的晶体
D. 元素W和M的某些单质可作为水处理中的消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
元素在周期表中的位置,反映了元素的原子结构和元素的性质。下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7∶17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
A.金属性:Y>Z B.氢化物的沸点:X>W
C.离子的还原性:X>W D.原子及离子半径:Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
考生注意:此题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
(A)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D. |
| 性质或结构信息 | 室温下单质呈粉末状固体,加热易熔化。 单质在氧气中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。 原子的M层上有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 原子最外电子层上s电子数等于p电子数 单质为空间网状晶体,具有很高的熔、沸点。 |
(1)B元素在周期表中的位置是____________,写出A原子的电子排布式 ____________。
____________。
(2)写出C单质与水反应的化学方程式_____________________。A与C形成的化合物溶于水后,溶液的pH____________7(填“大于”“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度__________(填“大”或“小”),其理由是____________________________________________________________________。
(4)A、B两元素非金属性较强的是(写元素符号)______________。写出能证明这一结论的一个实验事实________________________________________________________________。
(B)元素A—D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
| 元素 | A | B | C | D |
| 性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构。 | 单质常温、常压下是气体,原子的L层有一个未成对的p电子 | +2价阳离子的核外电子排布与氖原子相同 |
(1)上表中与A属于同一周期的元素是___________,写出D离子的电子排布式___________。
(2)D和C形成的化合物属于_______________晶体。
写出C单质与水反应的化学方程式_____________________________________________。
(3)对元素B的单质或化合物描述正确的是_______________。
a.B元素的最高正价为+6
b.常温、常压下单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是___________(写元素符号)。写出能证明该结论的一个实验事实_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指IA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答:
(1)A元素是__________、B元素是__________、C元素是__________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是__________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是__________。
(4)F是由两种元素组成的三原子分子,其分子式是__________,电子式是__________。
(5)G分子中含有4个原子,其分子式是__________。
(6)H分子中含有8个原子,其分子式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知对角线规则为:沿周期表中金属与非金属分界线方向对角的两主族元素性质相似,下列叙述中不正确的是
A.BeO为两性氧化物
B.Be(OH)2难溶于水
C.H3BO3是难溶于水的弱酸
D.B2O3既能溶于强酸又能溶于强碱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com