
【题目】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_________(填编号,下同),发生还原反应的是___________ 。(提示:铬元素化合价有+6、+3价)

(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。请回答下列问题:
①其中被还原的元素是________ ,氧化剂是__________ ,还原剂是_________ ,氧化产物是__________ ,还原产物是__________。
②表示反应中电子转移的方向和数目:__________。
10 A1 + 6 NaNO3 + 4 NaOH == 10 NaA1O2 + 3 N2↑ + 2 H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-═Cu2+;还原反应为:2Fe3++2e-═2Fe2+。
请据此将反应:Fe+2H+===Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________;还原反应为____________________。
【答案】④ ① N NaNO3 A1 NaA1O2 N2 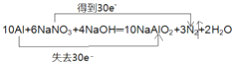 Fe-2e-=Fe2+ 【答题空10】2H++2e-=H2↑
Fe-2e-=Fe2+ 【答题空10】2H++2e-=H2↑
【解析】
(1)反应中①Cr元素化合价降低,发生还原反应;②③Cr元素化合价不变,发生非氧化还原反应;④Cr元素化合价升高,发生氧化反应;⑤Cr元素化合价不变,发生非氧化还原反应;故答案为:④;①;
(2)①Al元素的化合价升高,失去电子,Al被氧化,作还原剂,NaA1O2为氧化产物;NaNO3中N元素化合价降低得电子,被还原,作氧化剂,N2是还原产物,故答案为:N;NaNO3;Al;NaA1O2;N2;
②该反应中只有Al元素失电子化合价升高,Al元素化合价由0价变为+3价,所以10molAl完全反应转移电子的物质的量为30mol,则转移电子数为30NA;该反应中Al元素化合价由0价变为+3价,N元素化合价由+5价变为0价,根据方程式知,该反应中转移电子数是30,用双线桥表示电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
(3)根据化合价的变化判断,Fe+4H+=Fe2++ H2↑中,氧化剂是H+,发生还原反应,H+得到2个电子生成H2;还原剂是Fe,发生氧化反应,Fe失去2个电子生成Fe2+,电子转移数是2,故答案为:Fe-2e-=Fe2+;2H++2e-= H2↑。


科目:高中化学 来源: 题型:
【题目】由20g两种金属粉末组成的混合物,与足量的盐酸反应后得到标准状况下11.2L氢气,这种金属混合物的组成可能是( )
A. Mg和AlB. Fe和ZnC. Al和FeD. Zn和Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性.实验室可将氧气通过高压放电管来制取臭氧:3O2 ![]() 2O3 。
2O3 。
(1)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为________L。
(2)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g.则原混合气中臭氧的体积分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中不同的化学键如右图,关于其在各类反应中断裂键的说明不正确的是

A. 和金属钠反应键①断裂
B. 和HBr在一定条件下反应时键②断裂
C. 和浓硫酸共热140℃时键①或键②断裂;170℃时键②③断裂
D. 在Ag催化下和O2反应键①③断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为海水综合利用的部分流程,下列有关说法正确的是
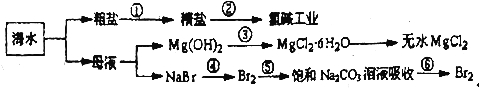
A. 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质加入的药品顺序为NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. 第②步是一个将电能转化为化学能的过程,工业上可采用石墨为电极,采用阴离子交换膜的电解装置
C. 第③步中结晶出的MgC12·6H2O可在空气中受热分解制无水MgC12
D. 第④步中反应的离子方程式为C12+2Br-=2C1-+Br2,第④⑤步的目的是富集溴元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L 1 mol·L-1的氨水中( )
A.含有1 mol NH3分子
B.含NH3和NH4+的物质的量之和为1 mol
C.含NH3·H2O、NH4+的物质的量之和为1 mol
D.含NH3、NH3·H2O、NH4+的物质的量之和为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图所示是分离混合物时常用的仪器,回答下列问题:

(1)写出仪器C、E的名称分别是_______________、______________。
(2)若向C装置中加入碘水和足量CCl4,充分振荡后静置,观察到现象是:C内液体分两层,上层液体呈________色,下层液体呈______________色。
(3)碘单质和溴单质有相类似的性质,都可以用有机溶剂萃取水溶液中的单质,若利用C仪器提取溴水中的溴单质,下列有机溶剂中不能选用的是_____________(填字母)。
A.汽油 B.CCl4 C.酒精 D.苯
Ⅱ.配制一定物质的量浓度的溶液是化学实验室的基本实验操作之一。请回答下列问题:
(1)配制0.5 mol/L的硫酸溶液450 mL,需用量筒量取质量分数98%、密度1.84 g/cm3的浓硫酸的体积为_____mL,如果实验室有15 mL、20 mL、50 mL 量筒,应最好选用_____mL量筒。
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的两种玻璃仪器是________________。
(3)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是__________(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)配制时,其正确的操作顺序是__________(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有水的烧杯中加入浓硫酸稀释
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(5)下面操作造成所配稀硫酸溶液浓度偏高的是___________(填序号)。
A.浓硫酸稀释后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量浓硫酸后洗涤量筒并将洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃在碱性醇溶液中能发生消去反应。
例如,![]()
该反应式也可表示为
下面是几种有机化合物的转化关系:

(1)根据系统命名法,化合物A的名称是_____________。
(2)反应①的反应类型_________,反应③的反应类型___________
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:_______。
(4)C2的结构简式是______________,F1的结构简式是______________,F1与F2互为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,炽热的铁与水蒸气在一个体积不变的密闭容器中进行反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
A. 把铁块变成铁粉B. 升高温度
C. 增加铁的量D. 增加水蒸气的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com