
(12分)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为 Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是____________(填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是____________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:____________________。
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是___________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体.高铁酸钾作为水处理剂发挥的作用是______________________。
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组离子在常温下一定能大量共存的是
A.pH=0的无色溶液中:Cl-、Na+、SO42-、Fe2+
B.在c(H+)/c( OH-) =1012的溶液中:NH4+、NO3-、K+、Cl-
C.加入铝粉能放出H2的溶液中:Mg2+、NH4+、NO3-、Cl-
D.含有大量Fe3+的溶液中:Al3+、SCN-、Br-、Na+
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 因为碳酸、氨水能够导电,所以液氨、二氧化碳是电解质
B. 由同种元素组成的物质一定是纯净物
C. 由C(石墨)=== C(金刚石);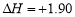 kJ·mol-1可知,石墨比金刚石稳定
kJ·mol-1可知,石墨比金刚石稳定
D. 在101kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为:2H2(g)+O2 (g) ===2H2O(l); 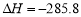 kJ·mol-1
kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
A.强酸溶液产生较多的氢气 B.两者产生等量的氢气
C.无法比较两者产生氢气的量 D.弱酸溶液产生较多的氢气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第一次月考化学试卷(解析版) 题型:填空题
(一)向一容积不变的密闭容器中充入一定量A和B,发生如下反应: x A(g) +2B(s) y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
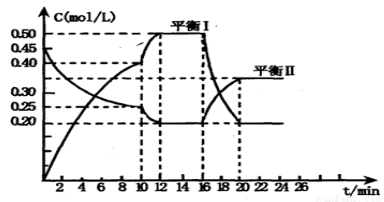
(1)0~l0min容器内压强____ (填“变大”,“不变”或“变小”)
(2)推测第l0min引起曲线变化的反应条件可能是 ;第16min引起曲线变化的反应条件可能是____ ;
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(3)若平衡I的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1 __________ K2(填“>”“=”或“<”)
(二) 尿素是蛋白质代谢的产物,也是重要的化学肥料。工业合成尿素反应如下:
2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图所示。

A点的正反应速率v正(CO2)_______B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);氨气的平衡转化率为________________________。
(2)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:2NH3(g)+CO2(g)  NH2COONH4(s) 关于上述反应的平衡状态下列说法正确的是________________
NH2COONH4(s) 关于上述反应的平衡状态下列说法正确的是________________
A.分离出少量的氨基甲酸铵,反应物的转化率将增大
B.平衡时降低体系温度,CO2的体积分数下降
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高氨基甲酸铵的产率
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期期中测试化学试卷(解析版) 题型:选择题
对下列物品标签的分析不正确的是
选项 | A | B | C | D |
物品标签 |
| 药品:×××
|
|
|
分析 | 该试剂应该装在橡胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 该物质受热易分解 | 该物质浓度为18.4mol/L |
查看答案和解析>>
科目:高中化学 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式不正确的是
A.向AgCl悬浊液中加入KI溶液:
B.明矾净水: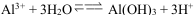
C.90℃时,测得纯水中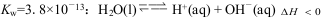
D.用热的纯碱溶液可以清洗油污:
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
既可用来除去甲烷中的丙烯,又可用来鉴别乙烷与丁烯的方法是
A.把气体通入足量液溴中
B.在导管口处点燃
C.一定条件下与H2发生加成反应
D.把气体通入足量溴水中
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高一上学期第一次月考化学试卷(解析版) 题型:选择题
在标准状况下,将1mol H2和11. 2 L O2混合,得到气体的体积为
A.12.2 L B.<22.4 L C.33.6 L D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com