
【题目】下列关于2甲基1丁烯[CH2=C(CH3)CH2CH3]的说法错误的是( )
A. 与1-丁烯(CH2=CHCH2CH3)互为同系物
B. 官能团有甲基、碳碳双键
C. 该有机物的所有碳原子可能共平面
D. 与环戊烷(![]() )互为同分异构体
)互为同分异构体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】可逆反应![]() ,在容积固定的密闭容器中达到平衡状态的标志是( )
,在容积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 表示的反应速率之比为
表示的反应速率之比为![]() 的状态
的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的物质的量不再改变的状态
A.①④⑥⑦B.②③⑤⑦C.①③④⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是黄绿色的气体(图中有些反应的产物和反应的条件没有全部标出)。

写出有关反应的离子方程式:
反应①_____。
反应②_____。
反应③_____。
(2)沉Co是用碳酸氢铵将![]() 中的
中的![]() 形成碳酸盐沉淀,试写出化学方程式:____。
形成碳酸盐沉淀,试写出化学方程式:____。
(3)铁硼矿(主要成分为![]() )可以制得硼酸,试写出铁硼矿与硫酸反应的化学方程式:___。
)可以制得硼酸,试写出铁硼矿与硫酸反应的化学方程式:___。
(4)工业上用软锰矿(主要成分![]() )制备锰酸钾。写出
)制备锰酸钾。写出![]() 、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:___。
、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:___。
(5)将氨气通入石灰乳,加入溴,于65℃进行反应也可制得溴化钙,此反应中还生成一种无色气体,写出反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲开展一次以化学为主题的活动,确定的课题是“研究浓硫酸与木炭粉在加热条件下反应的产物”。根据小组成员的推测,浓硫酸与木炭粉在加热条件下反应的产物可能有CO2、SO2,为了验证推测,小组讨论用以下装置进行实验:
编号 | a | b | c |
装置 |
品红 酸性KMnO4 品红 溶液 溶液 溶液 A B C |
|
|
请回答:
⑴ 实验时可观察装置a中A瓶溶液褪色,C瓶溶液不褪色。则A瓶溶液的作用___,C瓶溶液的作用_____;
⑵ 装置b中所加的液体是________,装置b可验证的产物是________;
⑶ 甲、乙两位同学分别设计了两套不同装置。甲的装置顺序:c→b→a,乙的装置顺序:c→a→b。你认为合理的是(填“甲”或“乙”)__;
⑷写出装置c中发生的化学方程式: __________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组制取氯气并进行氯气的性质实验,其装置如图所示,回答下列问题:
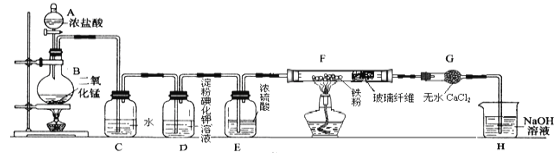
(1)仪器A的名称是 ______,实验中制备氯气的反应方程式为 ____________________。
(2)C中发生反应的化学方程式为 ______ .若将干燥的有色布条放入C中,观察到的现象是 ______,原因是 ___________________________。
(3)实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,写出D装置中发生反应的离子方程式______________________。
(4)F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解, 100℃左右时升华.双通管F中玻璃纤维(不参与反应)的作用是 ______ ;在F和H装置之间安装G装置的目的是____。
(5)H中NaOH溶液的作用是 _______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W在周期表中的相对位置如图,四种元素的原子最外层电子数之和为20。下列说法正确的是
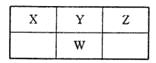
A.W位于第三周期ⅥA族
B.元素最高正价:Z>Y>X
C.简单气态氢化物稳定性:W>Y>X
D.工业上催化氧化Y的氢化物可用于制备其含氧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3OH 是一种无色有刺激性气味的液体,在生产生活中有重要用途。
Ⅰ.目前工业上有一种方法是用 CO2 生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:
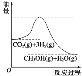
(1)你认为该反应为_____(填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是_____。
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2 充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=_____。
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是_____(填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学取V L浓缩的海水,用下图所示装置模拟工业法提溴。回答下列问题:
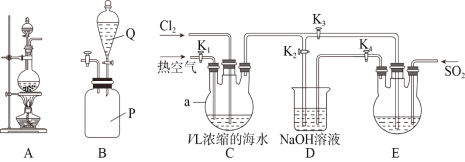
(1)装置A可用于实验室制备氯气,其反应原理为________________________________(用离子方程式表示),装置B是SO2贮气瓶,则Q中的溶液为________________。
(2)溴的富集过程:
①通入氯气与通入热空气的顺序是先通______________,通入氯气时K1、K2、K3的关、开方式是___________________。
②装置D的作用是_______________________________,通入SO2时装置E中发生反应的化学方程式为______________________________________。
(3)溴的精制:
①待装置E中Br-全部转化为单质后,再利用下图中的____________(填字母)装置进行蒸馏即可得到纯溴。
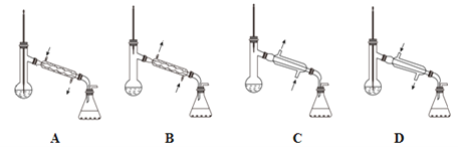
②假设最终得到m g纯溴,实验中溴的利用率为b%,则浓缩海水中c(Br-)=______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表回答下列问题:
(1)①表中实线是元素周期表的部分边界,请在图1中用实线补全元素周期表的边界________
②请画出金属与非金属的分界线________
③请在方框中(图3)按氦元素的式样写出h元素原子的相关信息________
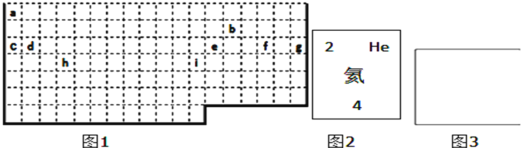
(2)X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31。
①X是______, Z是______(填写元素名称)
②X, Y, Z 三种元素的简单离子半径大小顺序是_____________________________
③三种元素形成的单质氧化性最强的化学式为______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com