
【题目】下列说法正确的是( )
A.CH3Cl(g)+Cl2(g)![]() CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
B.室温下,稀释0.1mol·L-1NH4Cl溶液,溶液中![]() 增大
增大
C.向稀氨水中加入少量氯化铵固体,一水合氨的电离程度增大
D.向硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,向沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
【答案】B
【解析】
A.反应CH3Cl(g)+Cl2(g)![]() CH2Cl2(l)+HCl(g)为熵减小的反应,该反应能自发进行,根据反应能否自发进行的判据可知ΔH-TΔS<0,ΔS<0,则ΔH<0,A错误;
CH2Cl2(l)+HCl(g)为熵减小的反应,该反应能自发进行,根据反应能否自发进行的判据可知ΔH-TΔS<0,ΔS<0,则ΔH<0,A错误;
B.氯化铵中铵根离子水解,溶液显酸性,加水稀释促进铵根离子水解,溶液中![]() 增大,B正确;
增大,B正确;
C.向稀氨水中加入少量氯化铵固体,溶液中铵根离子浓度增大,一水合氨的电离平衡逆向移动,一水合氨的电离程度减小,C错误;
D.向硫酸钡悬浊液中加入足量饱和Na2CO3溶液,使溶液中c(Ba2+)c(CO32-)> Ksp(BaCO3),产生碳酸钡沉淀,不能说明Ksp(BaSO4)、Ksp(BaCO3)的关系,D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】硼、镁及其化合物在工农业生产中应用广泛。
I.已知硼镁矿主要成分为![]() ,硼砂的化学式为
,硼砂的化学式为![]() 。一种利用硼镁矿制取金属镁及粗硼的工艺流程如下所示:
。一种利用硼镁矿制取金属镁及粗硼的工艺流程如下所示:
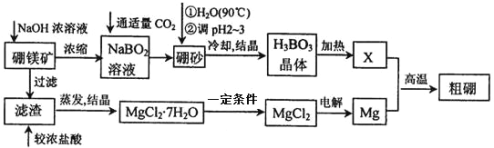
(1)写出硼元素在周期表中的位置_________________________
(2)将硼砂溶于热水后,用硫酸调节溶液的![]() 为23以制取硼酸
为23以制取硼酸![]() ,该反应的离子方程式为_________________________________________。
,该反应的离子方程式为_________________________________________。
(3)由![]() 制备
制备![]() 时,一定条件是_________________________________。
时,一定条件是_________________________________。
(4)制得的粗硼在一定条件下生成![]() ,
, ![]() 加热分解可以得到纯净的单质硼。现将
加热分解可以得到纯净的单质硼。现将![]() 粗硼制成的
粗硼制成的![]() 完全分解,将生成的
完全分解,将生成的![]() 配制成
配制成![]() 溶液,用酸式滴定管量取
溶液,用酸式滴定管量取![]() 碘水溶液放入锥形瓶中,向其中滴加几滴淀粉溶液,用
碘水溶液放入锥形瓶中,向其中滴加几滴淀粉溶液,用![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 。(提示:
。(提示:![]() )滴定终点的现象为____________,该粗硼样品的纯度为____________%
)滴定终点的现象为____________,该粗硼样品的纯度为____________%
Ⅱ (5)已知:![]() 的电离常数为
的电离常数为![]() ,
,![]() 的电离常数为
的电离常数为![]() 、
、![]() ,向盛有饱和硼酸溶液的试管中,滴加
,向盛有饱和硼酸溶液的试管中,滴加![]()
![]() 溶液,_____(填“能”或“不能”)观察到气泡逸出.
溶液,_____(填“能”或“不能”)观察到气泡逸出.
(6)![]() [也可写成
[也可写成![]() ]可以通过电解
]可以通过电解![]() 溶液的方法制备.工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过).
溶液的方法制备.工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过).

①![]() 膜为________交换膜(填“阴离子”或“阳离子”),写出产品室发生反应的离子方程式: ________________
膜为________交换膜(填“阴离子”或“阳离子”),写出产品室发生反应的离子方程式: ________________
理论上每生成![]() ,阴极室可生成________
,阴极室可生成________![]() 气体(标准状况)
气体(标准状况)
②![]() 室中,进口和出口的溶液浓度大小关系为
室中,进口和出口的溶液浓度大小关系为![]() ________
________![]() (填“>”或“<”)
(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
A. v(N2)=0.25 mol·L-1·min-1
B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=1 mol·L-1·min-1
D. v(NH3)=0.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL0.5mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是
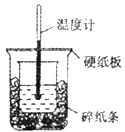
A.从实验装置上看,除了缺少环形玻璃搅拌棒外没有其他问题
B.大烧杯上如不盖硬纸板,测得的中和热数值会偏大
C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会偏大
D.实验中改用60mL0.5mol/L盐酸跟50mL0.55mol/LNaOH溶液进行反应,与上实验相比,所放出的热量不相等,但是所求中和热相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔在Pd表面选择加氢的反应机理如图所示。其中吸附在Pd表面上的物种用*标注。
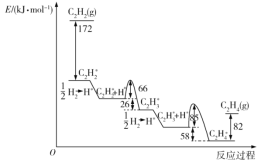
下列有关说法正确的是( )
A.该正反应历程中最大能垒(活化能)为85kJ·mol-1
B.吸附反应为吸热反应
C.Pd为固体催化剂,其表面积大小对催化效果无影响
D.C2H2*+H*→C2H3*只有化学键的形成过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,下列有关表述错误的是
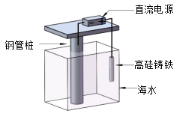
A.利用了电解原理
B.钢管桩上有刺激性气味气体生成
C.电子由电源负极流向钢管桩
D.高硅铸铁作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个体积均为2 L恒容密闭容器中,反应CO(g)+2H2(g)![]() CH3OH(g) ΔH<0达到平衡,得到如下数据。下列说法正确的是
CH3OH(g) ΔH<0达到平衡,得到如下数据。下列说法正确的是
容器编号 | 温度/K | 物质的起始物质的量/mol | 物质的平衡物质的量/mol | ||
CO(g) | H2(g) | CH3OH(g) | CH3OH(g) | ||
Ⅰ | T1 | 0.40 | 0.80 | 0 | 0.24 |
Ⅱ | T2 | 0 | 0 | 0.40 | 0.20 |
Ⅲ | T2 | a | b | ||
A.反应温度:T1<T2
B.达平衡时,转化率:α(CO,Ⅰ)+α(CH3OH,Ⅱ)>1
C.在容器Ⅲ中,若平衡时,CO的转化率大于H2,则![]()
D.在容器Ⅲ中,若起始时加入0.4 mol CO、0.4 mol H2和0.4 mol CH3OH,则此时v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雄黄![]() 酒,即是用研磨成粉末的雄黄泡制的白酒或黄酒,中华民族传统节日端午节的饮品。雌黄
酒,即是用研磨成粉末的雄黄泡制的白酒或黄酒,中华民族传统节日端午节的饮品。雌黄![]() 是工业制取高纯度砷的重要原料,下图是工业制纯砷流程:
是工业制取高纯度砷的重要原料,下图是工业制纯砷流程:
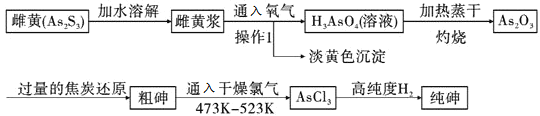
已知:砷在元素周期表中,位于硅元素相邻的右下角位置。
![]() 操作1的名称________。
操作1的名称________。
![]() 写出雌黄浆中通入氧气的化学方程式________。
写出雌黄浆中通入氧气的化学方程式________。
![]() 在粗砷的提纯过程中通常将温度控制在
在粗砷的提纯过程中通常将温度控制在![]() 以上,其目的是什么?________。
以上,其目的是什么?________。
![]() 在粗砷的提纯过程中,通入氯气这步操作为什么必须在干燥的环境中进行?________。
在粗砷的提纯过程中,通入氯气这步操作为什么必须在干燥的环境中进行?________。
![]() 写出
写出![]() 在灼烧条件下生成
在灼烧条件下生成![]() 的化学方程式:________。
的化学方程式:________。
![]() 砒霜的主要成分是
砒霜的主要成分是![]() ,古时候确定人是否砒霜中毒,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀硫酸,得到一种气体A,加热气体A,会得到单质砷。请写出A的化学式________。
,古时候确定人是否砒霜中毒,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀硫酸,得到一种气体A,加热气体A,会得到单质砷。请写出A的化学式________。
![]() 亚砷酸
亚砷酸![]() ,是三元弱酸,第一步和第二步产生
,是三元弱酸,第一步和第二步产生![]() 是通过和水中的氢氧根结合实现的,第三步则直接电离出
是通过和水中的氢氧根结合实现的,第三步则直接电离出![]() 。第一步电离方程式为:
。第一步电离方程式为:![]() ,第二步的电离方程式为________。
,第二步的电离方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com