��2010?����һģ��300��ʱ����2molA��2molB������������2L�ܱ������У��������·�Ӧ��3A��g��+B��g��

2C��g��+2D��g������H=Q.2minĩ�ﵽƽ�⣬����0.8mol D��
��1��300��ʱ���÷�Ӧ��ƽ�ⳣ������ʽΪ��K=
��
��֪K
300����K
350�������H
��
��
0���������������
��2����2minĩʱ��B��ƽ��Ũ��Ϊ
0.8mol/L
0.8mol/L
��D��ƽ����Ӧ����Ϊ
0.2mol/��L?min��
0.2mol/��L?min��
��
��3�����¶Ȳ��䣬��С�����ݻ�����A��ת����
����
����
�����������С�����䡱����ԭ����
��Ӧǰ������������䣬ѹǿ��ƽ����Ӱ��
��Ӧǰ������������䣬ѹǿ��ƽ����Ӱ��
��
��4���������ͬ�������£�������Ӧ���淴Ӧ������У���ʼʱ������C��D��
mol����ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����ԭ�ü���B
mol��

 2C��g��+2D��g������H=Q.2minĩ�ﵽƽ�⣬����0.8mol D��
2C��g��+2D��g������H=Q.2minĩ�ﵽƽ�⣬����0.8mol D�� 2C��g��+2D��g����
2C��g��+2D��g���� 2C��g��+2D��g����֪��C��D��
2C��g��+2D��g����֪��C��D��

 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д�
 ��2010?����һģ����һ������K2CO3��Һ�л����μ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬��Һ�и�������ĿҲ��Ӧ�ط����仯����Һ�и�������Ŀ��ͼ���������ߵĶ�Ӧ��ϵ��ȫ��ȷ���ǣ�������
��2010?����һģ����һ������K2CO3��Һ�л����μ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬��Һ�и�������ĿҲ��Ӧ�ط����仯����Һ�и�������Ŀ��ͼ���������ߵĶ�Ӧ��ϵ��ȫ��ȷ���ǣ�������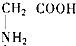 �У������������������Һ���ܷ�Ӧ���ǣ�������
�У������������������Һ���ܷ�Ӧ���ǣ�������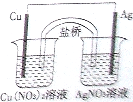 ��2010?����һģ����ͭƬ����Ƭ��Cu��NO3��2��Һ��AgNO3��Һ�����ߺ����ţ�װ����֬-KNO3��U�ιܣ�����һ��ԭ��أ���ͼ���������йظ�ԭ��ص�������ȷ����
��2010?����һģ����ͭƬ����Ƭ��Cu��NO3��2��Һ��AgNO3��Һ�����ߺ����ţ�װ����֬-KNO3��U�ιܣ�����һ��ԭ��أ���ͼ���������йظ�ԭ��ص�������ȷ����