
将35.8 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44 LNO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
A. 66.4 g B.50.8 g C 44.8g D. 39.2 g
【知识点】氧化还原反应中的规律 B3
【答案解析】B 解析:合金溶于足量的NaOH溶液中,金属铝和氢氧化钠反应产生气体氢气6.72L(标准状况),物质的量为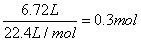 ,根据电子转移守恒可知n(Al)=0.2mol,故金属铝的质量为0.2mol×27g/mol=5.4g,金属铝提供电子的量是0.6mol,将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共提供电子的物质的量为
,根据电子转移守恒可知n(Al)=0.2mol,故金属铝的质量为0.2mol×27g/mol=5.4g,金属铝提供电子的量是0.6mol,将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共提供电子的物质的量为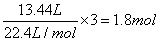 ,故Fe、Cu共提供的电子物质的量为1.8mol-0.6mol=1.2mol,向反应后的溶液中加入过量的NaOH溶液,所得沉淀为氢氧化铁、氢氧化铜,由电荷守恒可知,反应中金属铁、铜提供的电子的物质的量等于生成碱的氢氧根离子的物质的量,即n(OH-)=1.2mol,所以反应后沉淀的质量等于35.8g-5.4g+1.2mol×17g/mol=50.8g,
,故Fe、Cu共提供的电子物质的量为1.8mol-0.6mol=1.2mol,向反应后的溶液中加入过量的NaOH溶液,所得沉淀为氢氧化铁、氢氧化铜,由电荷守恒可知,反应中金属铁、铜提供的电子的物质的量等于生成碱的氢氧根离子的物质的量,即n(OH-)=1.2mol,所以反应后沉淀的质量等于35.8g-5.4g+1.2mol×17g/mol=50.8g,
【思路点拨】本题考查利用守恒方法进行简便计算,判断金属提供的电子的物质的量等于氢氧根的物质的量是该方法的关键,注意计算中守恒思想的运用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某温度下,对于反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
A.将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量 为92.4 kJ
为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增 大压强,H2的转化率增大
大压强,H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生做完实验后,采用下列方法清洗所用仪器:
①用浓氨水清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氧化钠溶液清洗盛过苯酚的试管
⑥用热氢氧化钠的浓溶液清洗沾有硫磺的试管
下列对以上操作的判断。正确的是 ( )
除①外都对 B.除⑥外都对 C.④⑤不对 D.全都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机化合物的结构简式为: ,下列有关该物质的叙述正确的是
,下列有关该物质的叙述正确的是
A. 1 mol该物质最多可以消耗3 mol Na
B.1 mol该物质最多可以消耗7 mol NaOH
C.不能与Na2CO3溶液反应
D.易溶于水,可以发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是
A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32-+H2O
B.Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+4H2O
C.磁性氧化铁溶于稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:
2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: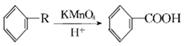 ,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
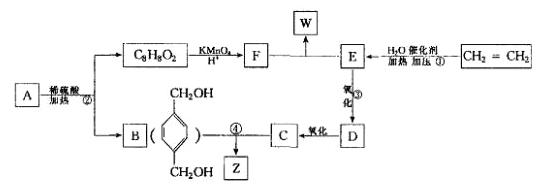
回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物有4种,其结构简式为_______________,_________________,_______________,______________。
(4)A的结构简式可能为_______________________________________(只写一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是
A.氯化铝溶液中加入过量的氨水:Al3++4 NH3·H2O=AlO2-+4 NH4+
B.稀硝酸中加入过量铁粉:Fe+4H++NO3- = Fe3++NO↑+2H2O
C.二氧化锰与浓盐酸混合加热:MnO2+4H++2Cl- △ Mn2++ Cl2↑+2H2O
D.石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏加德罗常数的值,下列说法正确的是
NA个Fe(OH)3胶体粒子的质量为107g
B.标准状况下,将2.24 L SO2溶于水中,溶液中H2SO3分子的数目是0.1NA
C.4.6 gN2O4和NO2的混合气体中含有的氧原子数为0.2NA
D.在含有2molH2SO4的浓硫酸中加入足量Zn粉,反应后转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3
B.反应Hg(1)+H2SO4(aq) = HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0
C.将纯水加热至较高温度,K变大、pH变小、呈酸性
D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com