
已知34Se和35Br位于同一周期,下列关系正确的是
| A.原子半径:Br>Se>Cl | B.热稳定性:HCl>H2Se>HBr |
| C.酸性:H2SeO4>HBrO4>HClO4 | D.还原性:Se2—>Br—>Cl— |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是
| A.原子序数: X<Y | B.原子半径:X<Y |
| C.离子半径:X>Y | D.原子最外层电子数:X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“玉兔”号月球车用 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于 Pu的说法正确的是
Pu的说法正确的是
A. Pu与 Pu与 U互为同位素 U互为同位素 | B. Pu与 Pu与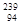 Pu互为同素异形体 Pu互为同素异形体 |
C. Pu与 Pu与 U具有完全相同的化学性质 U具有完全相同的化学性质 | D. Pu与 Pu与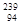 Pu具有相同的最外层电子数 Pu具有相同的最外层电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素R有如下反应:RO +5R-+6H+===3R2+3H2O,下列说法正确的是( )
+5R-+6H+===3R2+3H2O,下列说法正确的是( )
| A.元素R位于周期表中第ⅤA族 |
B.RO 中的R只能被还原 中的R只能被还原 |
C.每反应消耗1 mol RO ,转移电子的物质的量为5 mol ,转移电子的物质的量为5 mol |
| D.R2在常温常压下一定是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期。下列推测正确的是
| A.元素Y的最高化合价为+7 |
| B.三种元素的原子半径rZ>rY>rX |
| C.Z的单质比Y的单质更易与H2反应 |
| D.化合物X2Z2中阴阳离子数之比为1: 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素。下列说法中,错误的是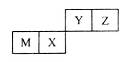
| A.Y元素气态氢化物的稳定性大于Z元素的 |
| B.M和Y两种元素,可以形成电子层结构相同的两种简单离子 |
| C.X元素最高价氧化物对应水化物的酸性弱于Y元素的 |
| D.M元素的氧化物既可以与酸溶液反应,也可以与碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等。则下列说法正确的是
A.B与A只能形成化合物BA3
B.C的原子半径、离子半径均分别小于D的原子半径、离子半径
C.A、B、C形成的化合物可能促进水的电离,也可能抑制水的电离
D.A、D均能与C形成原子个数比为1︰1、2︰1的化合物,且A2C2与D2C2的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质描述不正确的是( )
| A.在化合物中呈+2价 | B.单质能与水反应放出氢气 |
| C.镭比钙的金属性弱 | D.碳酸镭难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com