
【题目】室温下向10 mL 0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )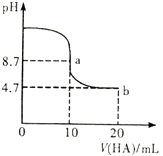
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
【答案】D
【解析】A、a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性,应为c(HA)>c(H+),A不符合题意;
B、a点A-水解,促进水的电离,b点时HA过量,溶液呈酸性,HA电离出H+ , 抑制水的电离,B不符合题意;
C、pH=7时,c(H+)=c(OH-),由电荷守恒可知c(Na+)+c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),C不符合题意;
D、b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA程度大于A-水解程度,则存在c(A-)>c(HA),D符合题意;
故答案为:DA.a点加入的HA的体积与NaOH溶液的体积相等,其反应后所得溶液的溶质为NaA,溶液显碱性;
B.a点中A-的水解会促进水的电离,b点中HA的电离会抑制水的电离;
C.pH=7时,c(H+)=c(OH-);
D.b点溶液中的溶质为NaA、HA,溶液显酸性,HA的电离大于A-的水解;


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素在元素周期表中的位置如图所示。
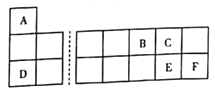
回答下列问题:
(1)在周期表中,E位于第_____________周期第_____________族。
(2)A、B能组成既含极性键又含非极性键的化合物,其电子式为_____________。
(3)在E、F的气态氢化物中,热稳定性较强的是_____________(填化学式,下同),还原性较强的是_______________。
(4)A、C、D、E组成两种酸式盐X、Y,将X、Y溶液混合发生复分解反应,写出离子方程式:________________________________________________________。
(5)常用(BA4)2E2C8检验废水中的Mn2+,若观察到无色溶液变紫红色,可判断废水中含Mn2+,还原产物与盐酸酸化的BaCl2溶液混合产生白色沉淀。写出无色溶液变紫红色溶液的离子方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是丁烷裂解的实验流程:(提示:丁烷在一定条件下裂解的可能方程式为:C4H10![]() C2H6+C2H4, C4H10
C2H6+C2H4, C4H10![]() CH4+C3H6)
CH4+C3H6)
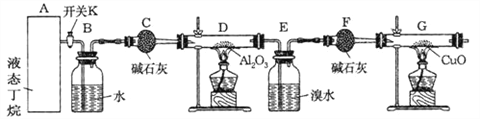
连接好装置后,需进行的实验操作有:
①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
(1)这三步操作的先后顺序依次是_______________________(填序号)
(2)写出甲烷与氧化铜反应的化学方程式______________________
(3)若对E装置中的混合物(溴水足量),再按以下流程实验:
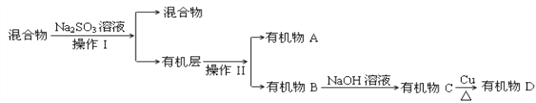
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ________Ⅱ________,Na2SO3溶液的作用是(用离子方程式表示)________________________________________________________.
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式_____________________.
(4)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7 g, G装置的质量减少了1.76 g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比 n(CH4): n(C2H6)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,可逆反应2SO2(g)+O2(g)![]() 2SO3(g)达到平衡的标志是
2SO3(g)达到平衡的标志是
A. SO2、SO3的浓度相等 B. 混合气体的密度保持不变
C. 混合气体的质量不再改变 D. 单位时间内消耗1molO2的同时,有2 mol SO3分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两根铁钉分别缠绕铜丝和铝条,放入滴有混合溶液的容器中,如图所示,下列叙述错误的是

A. b中铁钉附近呈现红色 B. a中铁钉附近呈现蓝色沉淀
C. b中发生吸氧腐蚀 D. a中铜丝附近有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于右图所示转化关系(X代表卤素)的说法错误的是:
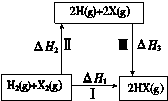
A.2H(g) +2X(g) = 2HX(g) ΔH3<0
B.ΔH1 = ΔH2 + ΔH3
C.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量按Cl、Br、I的顺序依次增多
D.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是( )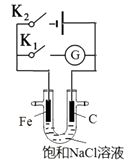
A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com