
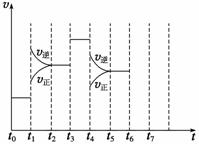
利用如图所示装置进行下列实验,能得出相应实验结论的是
| 选项 | ① | ② | ③ | 实验结论 |
|
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
一些烷烃的燃烧热如下表:
| 化合物 | 燃烧热/(kJ/mol) | 化合物 | 燃烧热/(kJ/mol) |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 2—甲基丁烷 | 3 531.3 |
下列表达正确的是( )
A.正戊烷的燃烧热大约在3 540 kJ/mol左右
B.热稳定性:正丁烷<异丁烷
C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)===4CO2(g)+6H2O(l) ΔH=-1 560.8 kJ/mol
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
将甲烷与氯气混合,在光照下充分反应,所得产物有:①CH3Cl,②CH2Cl2,③CHCl3,④CCl4,⑤HCl。其中正确的是 ( )
A.①⑤ B.②⑤ C.①②③的混合物 D.①②③④⑤的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸。乳酸最初就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为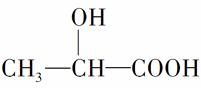 。完成下列问题:
。完成下列问题:
(1)写出乳酸分子中官能团的名称:______、______。
(2)写出乳酸与足量金属钠反应的化学方程式:
_____________________________________________________。
(3)写出乳酸与碳酸钠溶液反应的化学方程式:
_____________________________________________________。
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此生成物的结构简式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1814年戴维发现了一氯化碘(ICl)、三氯化碘(ICl3),由于它们的性质与卤素相似,因此被称为卤素互化物。
(1)氯元素在元素周期表中的位置是_________;ICl的电子式为____________。
(2)ICl与冷的NaOH稀溶液反应的离子方程式为____________________。
(3)用海带制碘时,生成的粗碘中常混有ICl,可加入KI加热升华提纯,发生化学反应的化学方程式为_____________________。
(4)三氯化碘常以二聚体I2Cl6的形式存在,经电导仪测定知,它能发生部分电离,生成的两种离子的相对质量分别为198和269,其电离方程式为_________________________。下列说法正确的是______。
a.ICl3分子中各原子均达到8电子稳定结构
b.由反应KClO3+I2+6HCl=2ICl3+KCl+3H2O,可知还原性:KClO3>ICl3
c.ICl与乙烯反应的化学方程式为CH2=CH2+ICl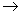 ICH2CH2Cl
ICH2CH2Cl
d.ICl与苯反应制取碘苯的化学方程式为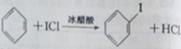
查看答案和解析>>
科目:高中化学 来源: 题型:
易燃易爆有毒的化学物质在其包装上应贴上危险警告标签。下列物质贴错了标签的是
| A | B | C |
| |
| 物质的化学式 | 浓H2SO4 | CCl4 | P4 | NH4NO3 |
| 危险警告标签 | 腐蚀品 | 易燃品 | 剧毒品 | 爆炸品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素;少量A与水反应可完全水解而不被氧化或还原,所有反应产物均可溶于水;将A配成水溶液稀释后 分成几份,分别加入一系列的试剂,现象如下:
分成几份,分别加入一系列的试剂,现象如下:
①加入硝酸和硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀生成;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀;
(1)由此判断组成该化合物的元素中,可能存在的卤素有____________,A与水反应后生成的溶液中含有的离子可能有_________________________。
(2)要确定该化合物的分子式,称取11.90g A溶于水稀释至250.0mL,取25.00mL溶液加入足量的高锰酸钾溶液和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重,为2.33g,试确定A的化学式,写出计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1) m+n_________p(填“>”“=”“<”)。
(2)若加压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
 (3)若加入A(体积不变),则B的转化率_________。
(3)若加入A(体积不变),则B的转化率_________。
(4)若降低温度,则平衡时B、C的浓度之比 将______ ___。
(5)若加入催化剂,平衡时气体混合物的总物质的量____ _____。
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色____ (填“变深”“变浅”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com