
易燃易爆有毒的化学物质在其包装上应贴上危险警告标签。下列物质贴错了标签的是
| A | B | C |
| |
| 物质的化学式 | 浓H2SO4 | CCl4 | P4 | NH4NO3 |
| 危险警告标签 | 腐蚀品 | 易燃品 | 剧毒品 | 爆炸品 |
科目:高中化学 来源: 题型:
氨在国民经济中占有重要的地位,请参与下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。
C(s)+H2O(g)H2(g)+CO(g)
ΔH=+131.3 kJ,ΔS=+133.7 J/K
该反应在低温下能否自发反应__________(填“能”或“否”)。
(2)已知在400℃时,N2(g)+3H2(g)2NH3(g)的K′=0.5。
①2NH3(g)N2(g)+3H2(g)的K=__________(填数值)。
②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v(N2)正__________v(N2)逆(填“>”、“<”、“=”或“不确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列几组物质(将正确答案字母填入空中)
A.金刚石和石墨 B.C2H6和C5H12 C.C2H4和C2H6
D.CH3CH2CH2CH3和CH3CH(CH3)2 E.35Cl和37Cl
属于同分异构体的是________;属于同素异形体的是_______;属于同系物的是________;属于同位素的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示装置进行下列实验,能得出相应实验结论的是
| 选项 | ① | ② | ③ | 实验结论 |
|
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
无机化合物A中含有元素Li元素,A的摩尔质量23g·mol-1,A主要用于有机合成和药物制造,同时也是良好的储氢材料。在一定条件下,0.1mol固体A与0.1molNH4Cl固体恰好完全反应,生成固体B和4.48L(标准状况)气体C。已知气体C极易溶于水,且得到碱性溶液。电解无水B可生成金属单质D和氯气。请回答下列问题:
(1)A的化学方式是_________________________。
(2)写出化合物A与NH4Cl反应的化学方程式:_______________________________。
(3)某同学通过查阅资料得知物质A的性质:
I.工业上可用金属D与液态的C在硝酸铁催化下反应来制备A物质。
II.物质A遇水强烈水解,释放出气体C。
①I中发生反应的基本反应类型是__________________________。
②物质A遇水强烈水解的化学方程式为_________________________。
(4)工业制备单质D的流程如下:
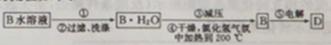
①步骤①中操作的名称为________________。
②试用平衡原理解释步骤③中减压的目的是:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②碱性氧化物一定是金属氧化物
③根据丁达尔现象可将分散系分为胶体、溶液和浊液
④SiO2是酸性氧化物,能与NaOH溶液反应
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
A. ②③ B.②④⑤ C.①②④ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
A.加入合金的质量可能为9.6g
B.沉淀完全时消耗NaOH溶液体积为150mL
C.参加反应的硝酸的物质的量为0.4mol
D.溶解合金时产生NO气体体积0.224L(以标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备是:
I. 将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2,制得混有SiCl4杂质的TiCl4。
II. 将混有SiCl4杂质的TiCl4分离,得到纯净的TiCl4。
III. 在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O。
IV. TiO2·xH2O高温分解得到TiO2。
①TiCl4与SiCl4在常温下的状态是_______。II中所采取的操作名称_______。
|

②如实验IV中,应将TiO2.xH2O放在_______ (填仪器编号)中加热。
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a. O2→2O b. O+H2O→2OH(羟基) c. OH+OH→H2O2
①b中破坏的是 (填“极性共价键”或“非极性共价键”)。
②H2O2能清除路面空气中的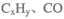 等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
(3)过氧化氢是重要的化学试剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量。
请填写下列空白:
①取10.00 mL密度为P g/mL的过氧化氢溶液稀释至250 mL。取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数配平及化学式填写在方框里。
 MnO+ H2O2+ H+= Mn2++ H2O+
MnO+ H2O2+ H+= Mn2++ H2O+
②滴定时,将高锰酸钾标准溶液注入______________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是____________________________。
③重复滴定三次,平均耗用C mol/L KMnO4标准溶液 V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________ (填“偏高”或“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,浓度都为1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,4 s后X2、Y2、Z的浓度分别是0. 4 mol·L-1,0.8 mol·L-1,0.4 mol·L-1,如Z用X、Y表示,则该反应式是( )
A.X2+2Y2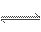 2XY2 B.2X2+Y2
2XY2 B.2X2+Y2 2X2Y
2X2Y
C.3X2+Y2 2X3Y D.X2+3Y2
2X3Y D.X2+3Y2 2XY3
2XY3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com