
【题目】一定条件下,将一定体积的H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含amol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含有Cl﹣、ClO﹣、ClO3﹣且三者物质的量之比为8:1:1,则:
(1)原混合气体中Cl2的物质的量为(用含a的数学式表示).
(2)氢气和氯气的物质的量之比为 .
【答案】
(1)![]() amol
amol
(2)1:5
【解析】解:(1)混合气体通入含amolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl﹣、ClO﹣、ClO﹣3 , 根据电荷守恒可知,溶液中n(Na+)=n(Cl﹣)+n(ClO﹣)+n(ClO﹣3),根据氯元素守恒可知,
H2和Cl2的混合气体中n(Cl2)= ![]() [n(Cl﹣)+n(ClO﹣)+n(ClO﹣3)]=
[n(Cl﹣)+n(ClO﹣)+n(ClO﹣3)]= ![]() n(Na+)=
n(Na+)= ![]() amol,
amol,
所以答案是: ![]() amol;(2)混合气体通入含amolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl﹣、ClO﹣、ClO﹣3 , 根据电荷守恒可知,溶液中n(Na+)=n(Cl﹣)+n(ClO﹣)+n(ClO﹣3),
amol;(2)混合气体通入含amolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl﹣、ClO﹣、ClO﹣3 , 根据电荷守恒可知,溶液中n(Na+)=n(Cl﹣)+n(ClO﹣)+n(ClO﹣3),
由于溶液中Cl﹣、ClO﹣、ClO﹣3三者的物质的量之比为8:1:1,所以溶液中n(Cl﹣)= ![]() amol,n(ClO﹣)=
amol,n(ClO﹣)= ![]() amol,n(ClO﹣3)=
amol,n(ClO﹣3)= ![]() amol,
amol,
令氯气与氢氧化钠反应生成的氯离子的物质的量为xmol,根据电子转移守恒有x= ![]() a+
a+ ![]() amol×5=
amol×5= ![]() amol,
amol,
溶液中Cl﹣来源于氯化氢及氯气与氢氧化钠的反应,所以氯化氢提供的氯离子为 ![]() amol﹣
amol﹣ ![]() amol=
amol= ![]() mola,
mola,
即反应后的混合气体中n(HCl)= ![]() amol,根据氢元素守恒可知,n(H2)=
amol,根据氢元素守恒可知,n(H2)= ![]() n(HCl)=
n(HCl)= ![]() ×
× ![]() mola=0.1amol,
mola=0.1amol,
则氢气和氯气的物质的量之比0.1a:0.5a=1:5,
所以答案是:1:5.
【考点精析】利用氯气的化学性质对题目进行判断即可得到答案,需要熟知氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


科目:高中化学 来源: 题型:
【题目】常见有机物间的转化关系如图所示(以下变化中,某些反应条件及产物未标明).A是天然有机高分子化合物,D是一种重要的化工原料.在相同条件下,G蒸气密度是氢气的44 倍. 
(1)D中官能团的名称: .
(2)C和E反应的化学方程式: .
(3)检验A转化过程中有B生成,先中和水解液,再需要加入的试剂是 .
(4)某烃X的相对分子质量是D、F之和,分子中碳与氢的质量之比是5:1.
下列说法正确的是
A.X 不溶于水,与甲烷互为同系物
B.X性质稳定,高温下不会分解
C.X不存在含有3个甲基的同分异构体
D.X可能和溴水发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在烧瓶放20克蔗糖,依次加入少量水、20mL浓硫酸,蔗糖逐渐变黑,体积膨胀,形成疏松多孔的黑面包,烧瓶发烫,品红溶液颜色变淡.请回答: 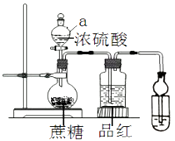
(1)仪器a的名称
(2)小试管盛装试剂
(3)下列说法不正确的是
A.蔗糖变黑说明发生过程 C12H22O11→C+H2O
B.品红颜色变淡说明SO2有漂白性
C.上述实验体现浓硫酸的脱水性、吸水性和氧化性
D.将气体依次通过饱和碳酸氢钠溶液、澄清石灰水,石灰水变浑浊证明含有CO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体数目的叙述中,不正确的是( )
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.结构简式为 ![]() 的烃,分子中含有两个苯环的该烃的同分异构体为4种
的烃,分子中含有两个苯环的该烃的同分异构体为4种
C.碳原子数小于或等于10的烷烃中其一氯代物只有一种的烷烃有4种
D.菲的结构简式为 ![]() ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4 . 某同学用15.0g该废催化剂为原料,回收锌和铜.采用的实验方案如下,回答下列问题: 
已知:ZnS与稀硫酸反应,且化合价不变; CuS既不溶解于稀硫酸,也不与稀硫酸反应
(1)在下列装置中,第一次浸出反应装置最合理的(填标号). 
(2)滤液1中含有Fe2+ , 选用提供的试剂进行检验,检验方法如下: .
(提供的试剂:稀盐酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水)
(3)本实验要用到抽滤,设所用的洗涤剂为X,抽滤洗涤沉淀的操作 .
(4)写出第二次浸出的化学反应方程式 , 向盛有滤渣1的反应器中加H2SO4和H2O2溶液,应先加 .
(5)滤渣2的主要成分是 . 浓缩、结晶得到硫酸锌晶体的主要仪器名称是 .
(6)某同学在实验完成之后,得到1.50g CuSO45H2O,则铜的回收率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是三种常见有机物的比例模型示意图.下列说法正确的是( )
A.甲在光照条件下与Cl2反应可得到四种不同的产物
B.乙、丙所有的原子均处于同一平面,均可使溴水反应褪色
C.石油分馏可获得甲和乙,煤干馏可获得丙
D.在浓硫酸存在下,丙与浓硝酸共热的反应属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质.已知:甲+乙=丁+己,甲+丙=戊+己; 丁溶液为短周期元素中最高价氧化物对应水化物中碱性最强的物质.下列说法正确的是( )
A.原子半径:W>Z>Y>X
B.Y元素在周期表中的位置为第三周期第ⅣA族
C.1mol甲与足量的乙完全反应共转移了1mol电子
D.甲、乙、丙、丁、戊、己中含有的共价键的物质只有乙、丙、己
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com