
| A. | Q1+Q2>Q3 | B. | Q1+Q2<Q3 | C. | Q1+Q2>2Q3 | D. | Q1+Q2<2Q3 |
分析 根据反应热△H=反应物的总键能-生成物的总键来计算该反应的反应热,氢气在氯气中燃烧,反应热△H<0,据此进行解答.
解答 解:破坏1molH2中的化学键消耗的能量为Q1kJ,则H-H键能为Q1kJ/mol,
破坏1molCl2中的化学键消耗的能量为Q2kJ,则Cl-Cl键能为Q2kJ/mol,
形成1molHCl中的化学键释放的能量为Q3kJ,则H-Cl键能为Q3kJ/mol,
反应H2(g)+Cl2(g)═2HCl(g)的焓变:△H=反应物的总键能-生成物的总键能=Q1kJ/mol+Q2kJ/mol-2Q3kJ/mol=(Q1+Q2-2Q3)kJ/mol,
由于氢气在氯气中燃烧,反应热△H<0,即(Q1+Q2-2Q3)<0,
所以Q1+Q2<2Q3,
故选D.
点评 本题考查反应热与焓变的应用,题目难度不大,注意把握从键能的角度计算反应热的方法,明确化学反应与能量变化的关系为解答关键.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
同温同压下,两种气体的体积如果不相同,请你推测其主要原因是( )
A.气体的分子大小不同 B.气体的物质的量不同
C.气体分子的化学性质不同 D.气体分子间的平均距离不同
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
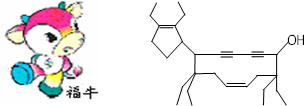
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
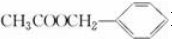 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
 ,B中含氧官能团的名称是羧基.
,B中含氧官能团的名称是羧基.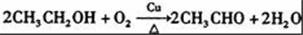 ;
;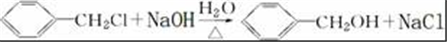 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com