
����Ŀ����ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��xA(g)+B(g) ![]() 2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ
2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ
���� | �� | �� | �� |
�ݻ� | 0.5L | 0.5L | 1.0L |
�¶ȣ��� | T1 | T2 | T2 |
��Ӧ����ʼ�� | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |

����˵����ȷ����
A.��ͼ��֪��T1��T2���Ҹ÷�ӦΪ���ȷ�Ӧ
B.T2ʱ�÷�Ӧ��ƽ�ⳣ��K=0.8
C.l0min�ڼ������з�Ӧ��ƽ������v(B)=0.025mol��(L��min)��1
D.T1�棬����ʼʱ�������г���1.5molA��0.5molB��ƽ��ʱB��ת����Ϊ25%
���𰸡�B
��������
A����ͼ��֪���ҷ�Ӧ���ʿ죬�¶ȸߣ�T1��T2������C��Ũ�ȵͣ��¶ȸ߷�Ӧ������У���ӦΪ���ȷ�Ӧ��A����
B���ɱ����ҡ�����֪������������������ʵ�����ԭ����4����ƽ��ʱ����C��Ũ�����ҵ�2����˵����������ı䣬ƽ�ⲻ�ƶ�����x=1��ƽ��ʱ����A��B��C��Ũ�ȷֱ��ǣ�mol/L��0.5��2.5��1������ƽ�ⳣ��K=12/(0.5��2.5)=0.8��B��ȷ��
C��l0min�ڼ������з�Ӧ��ƽ������v(C)=0.1mol��(L��min)��1����v(B)=0.05mol��(L��min)��1��C����
D��T1�棬����ʼʱ�������г���1.5molA��0.5molB�������0.5molA��1.5molB�ǵ�Ч�ģ�A��B��������ͬ��������ƽ��ʱC������Ϊ0.75mol����Ӧ��n(B)=n(C)��2=0.375mol������B��ת����Ϊ0.375/0.5��100%=75%��D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���º�ѹ���ܱ������з������·�Ӧ��A(g)+B(g)2C(g) ��H<0��t1ʱ�̴ﵽƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ��ʾ������˵������ȷ���ǣ� ��

A.0��t2ʱ��v(��)>v(��)
B.�������̴ﵽƽ��ʱ��A�����������=��
C.t2ʱ�̸ı�����������ܱ������м�C
D.�������̴ﵽƽ��ʱ��ƽ�ⳣ��K(��)=K(��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ǰ������Ԫ��A��B��C��D��E��Fԭ��������������������������±���ʾ��
A | 2p�ܼ����Ӱ���� |
B | ��Aͬ���ڣ���ԭ�Ӻ�����2��δ�ɶԵ��� |
C | ��̬ԭ�Ӻ�����6��ԭ�ӹ�����е��ӣ���ֻ��1��δ�ɶԵ��� |
D | ���̬ԭ����Χ�����Ų�Ϊmsnmpn��2 |
E | ǰ������Ԫ���У�EԪ�ػ�̬ԭ��δ�ɶԵ�������� |
F | ��̬F�����ܼ�����ȫ���� |
���������������ش��������⣺
��1��EԪ�ػ�̬ԭ�Ӻ�����__��������ͬ�ĵ��ӣ������Ų�ʽΪ__������FԪ�ػ�̬ԭ�ӵļ۵����Ų�ͼ___��
��2����B���ڵ�ͬ����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ___��(��Ԫ�ط��ű�ʾ)
��3��B��C��D����Ԫ�صļ����ӵİ뾶��С�����˳��Ϊ___(�����ӷ��ű�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�pH=12���������ƺ�pH=4�Ĵ���������Ϻ�ǡ���кͣ����Ի�Ϻ���Һ����ı仯������˵������ȷ����
A.��Ϻ����Һ������B.���ǰ����Һ��ˮ�ĵ���̶Ȳ�ͬ
C.�������ƺʹ����Ũ�Ȳ����D.���ǰ�Ĵ���Լ1%��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º�ѹ�ܱ�����M����ͼ�ͺ��º����ܱ�����N����ͼ���У��������о�����a molA��a molB����ʼʱ�����������ΪVL���������·�Ӧ���ﵽ��ѧƽ��״̬��2A��?��+ B��?��![]() xC��g�� ��H��0��ƽ��ʱM��A��B��C�����ʵ���֮��Ϊ1��3��4�������жϲ���ȷ����
xC��g�� ��H��0��ƽ��ʱM��A��B��C�����ʵ���֮��Ϊ1��3��4�������жϲ���ȷ����

A. x��2
B. ��N��������ܶ���ͼ����ʾ����A��Bֻ��һ������̬
C. AΪ���壬BΪ�����壬��ƽ��ʱM��N��C�����ʵ������
D. ��A��B��Ϊ���壬ƽ��ʱM��A��ת����С��N��A��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������Ϊ����������ƹ㷺Ӧ�����ν�Ⱦ�ϡ�Ƥ���Ƶȹ�ҵ�����Ƶ�һ���Ʊ�������Na2SO4+2C![]() Na2S+2CO2���������й�˵����ȷ����
Na2S+2CO2���������й�˵����ȷ����
A. 1L.0.25mol/L.Na2SO4��Һ�к��е���ԭ����ĿΪNA
B. 1L.0.1mol/LNa2S��Һ�к��е���������ĿС��0.1NA
C. ����1mol��ԭ����ʱת�Ƶ�����Ϊ8NA
D. ͨ��״���£�11.2L.CO2�к��еĹ��ۼ���ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ������˵����ȷ����
A. 2gD2O��H2l8O�����������������ΪNA
B. 1L0.1mol��L-1 NaHCO3��Һ��HCO3-��CO32-������֮��Ϊ0.1NA
C. ���³�ѹ�£�0.5 mol Fe������Ũ�����ϣ�ת�Ƶ�����Ϊ1.5NA
D. 0.1 mol H2��0.1 mol I2 (g)���ܱ������г�ַ�Ӧ����ԭ������Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�ʱ������������Ӧ���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1= -99kJmol-1
CH3OH(g) ��H1= -99kJmol-1
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H2= 58kJmol-1
CH3OH��g��+H2O(g) ��H2= 58kJmol-1
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3=+41kJmol-1
CO(g)+H2O(g) ��H3=+41kJmol-1
��1��һ���¶��£������Ϊ2L���ܱ������м���CO��H2������ֻ������Ӧ�٣���ƽ����ø����Ũ�����£�
���� | CO | H2 | CH3OH |
Ũ��(molL-1) | 0.9 | 1.0 | 0.6 |
����ʽ������ƽ�ⳣ��K=___��
�������������ѹ��Ϊ1L���������㣬Ԥ����ƽ����c(H2)��ȡֵ��Χ��___��
��������������䣬�ٳ���0.6molCO��0.4molCH3OH����ʱv��__v��(�>������<����=��)��
��2����ʵ�������У����ϳ��������n(H2)/n(CO+CO2)=2.60ʱ��ϵ�е�COƽ��ת������(CO)���¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
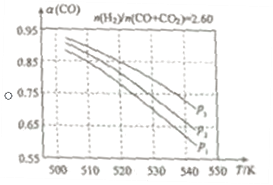
����CO��ֵ���¶����߶�___�������С��������ԭ����___��ͼ�е�ѹǿ�ɴ�СΪ___�����ж�������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���淴Ӧ��ij���Ϊ5L���ܱ������н������ڴ�0~3���Ӹ����ʵ����ı仯�����ͼ��ʾ(A��B��C��Ϊ����)
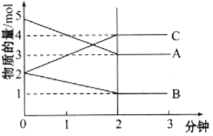
��1���÷�Ӧ�Ļ�ѧ����ʽΪ__________________��
��2����һ���¶��������������ܱ���������������Ӧ�ﵽƽ��ı�־��___________(����ĸ)��
A.�������������ֲ��� B.A��B��C��Ũ�ȶ����
C.A��B��C��Ũ�Ȳ��ٷ����仯 D.A��B��C�ķ�����֮��Ϊ2:1:2
E.����Ӧ���淴Ӧ����ֹͣ F.�����������ܶȲ��ٷ����仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com