
A~F均为元素周期表中前四周期元素,其相关信息如下表:
元素 | 相 关 信 息 |
A | A的基态原子最外层电子排布式为2s22p3 |
B | B是地壳中含量最高的元素 |
C | C+与B的简单离子的电子层结构相同 |
D | D的一种核素的质量数为64,中子数为35 |
E 、F | E 、F既同周期又同族,且原子序数F比E多2 |
请回答下列问题:
(1)D的价电子的电子排布式是 ;F原子的原子结构示意图为 。
(2)A、B的第一电离能的大小顺序为 。
(3)AB3-中A原子的杂化轨道类型为_____;与A2B互为等电子体的分子的分子式为 (任写一个即可)。
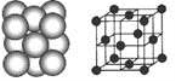
(4) D晶体的晶胞如图所示为面心立方最密堆积(在晶胞的顶点和面心均含有一个D原子)。则D的晶体中D原子的配位数为 。
(5)已知17gA的简单氢化物催化氧化生成气态水时放出QkJ的热量,请写出A的简单氢化物催化氧化的热化学反应方程式 。
(6)C2B2的电子式为____;它可与E的二氯化物溶液反应,若反应的C2B2与E的二氯化物的物质的量之比为1:2,则该反应的化学反应方程式为 。
(1)3d104s1 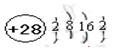
(2)N大于O
(3)sp2 CO2
(4)12
(5)4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-Q kJ/mol
(5)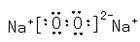 3Na2O2+6FeCl2+6H2O=6NaCl+4Fe(OH)3↓+2FeCl3
3Na2O2+6FeCl2+6H2O=6NaCl+4Fe(OH)3↓+2FeCl3
【解析】由题知,A的基态原子最外层电子排布式为2s22p3,A是N元素;B是地壳中含量最高的元素,B是O;C+与B的简单离子的电子层结构相同,C是Na;D的一种核素的质量数为64,中子数为35,D是Cu;E 、F既同周期又同族,则它们两是第四周期Ⅷ,且原子序数F比E多2,E、F分别是Fe、Ni。
(1)Cu的价电子除了4s上电子外,还包括3d上的电子;
(2)N的2p处于半充满状况,N第一电离能大于O;
(3)AB3-中N的孤电子对对数=(5+1-3×2)/2=0,即采取sp3,与N2O互为等电子体是CO2;
(4)同一个切面上的对角线顶点4个,共3个面,共12个。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)1.1中和反应反应热的测定(解析版) 题型:选择题
已知强酸与强碱的稀溶液发生中和反应的热化学方程式为:H+(aq)+OH-(aq) H2O(l) ΔH=-57.3 kJ·mol-1,又知电解质的电离是吸热过程。向1 L 0.5 mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应。其焓变ΔH1、ΔH2、ΔH3的关系是( )
H2O(l) ΔH=-57.3 kJ·mol-1,又知电解质的电离是吸热过程。向1 L 0.5 mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应。其焓变ΔH1、ΔH2、ΔH3的关系是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH3<ΔH2 C.ΔH1=ΔH3>ΔH2D.ΔH1>ΔH3>ΔH2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学铁及其化合物主要性质(解析版) 题型:选择题
下列有关金属及其化合物的说法正确的是
A.Mg和Al都可以用电解法冶炼得到
B.Na2O2、Na2O组成元素相同,与CO2反应产物也相同
C.用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3
D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学速率表示与平衡移动(解析版) 题型:实验题
某化学小组设计如图实验装置
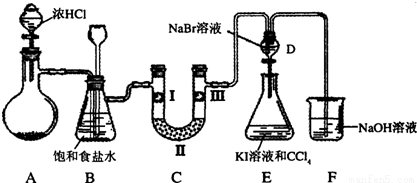
(1)若装置A中的固体药品为KClO3,则写出离子方程式 。
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞。若C中发生堵塞,B中将观察到的现象是 。
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是 , 。
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。请简述能说明氯、溴、碘非金属性强弱的实验操作及现象 。(夹持装置略去)制备Cl2并探究氯气的相关性质:
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学速率表示与平衡移动(解析版) 题型:选择题
使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)。下列说法错误的是
2NH3(g)(正反应为放热反应)。下列说法错误的是
A.升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大
B.升高平衡体系的温度(保持体积不变),混合气体的密度不变
C.当反应达到平衡时,N2和H2的浓度比是1∶3
D.当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习5(解析版) 题型:填空题
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):

填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是 。
(2)上述流程中,工业上分离H2 、CO2合理的方法是 。
A混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B混合气加压冷却,使CO2液化
C混合气用氨水洗涤
D混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行 ,目的是____________________;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法 。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,阐述图中的两处可以合理利用资源情况 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习4(解析版) 题型:填空题
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)写出Ti基态原子的电子排布 。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C B(选填“>”“<”),第一电离能N>O,原因是 。
(3)月球岩石玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。SO42-的空间构型为 ,其中硫原子采用 杂化,氧原子的价电子排布图为 ,任意写出一种SO42-等电子体 。
(4)将TiOSO4的稀溶液加热水解后,经进一步反应,可得到钛的某种氧化物。该氧化物的晶胞结构图如图所示。
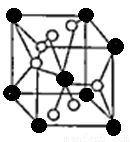
则该氧化物的化学式 (图中钛原子用“O”表示。氧原子用“O”表示)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习2(解析版) 题型:填空题
废旧锂离子池的正极材料(主要含有LiCoO2及少量的Al、Fe等)可用于回收钴、锂,工艺流程如下:
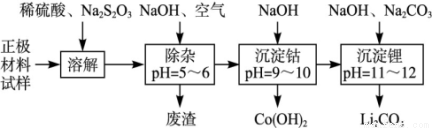
(1)在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中发生反应的化学方程式为 ,还原产物是 。
(2)在上述除杂过程中,通入空气的作用是 废渣的主要成分是 。
(3)“沉淀钴”和“沉淀锂”的离子方程式分别为 。
(4)除了废渣可以回收利用外,本工艺还可回收的副产品是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式的书写及正误判断(解析版) 题型:选择题
下列有关的离子方程式正确的是
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O= +4
+4
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液:
C.磷酸一氢钠溶液水【解析】 +H2O
+H2O
 +H3O+
+H3O+
D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com