
| A�� | �տ�ʼ��Ӧʱ���ʣ��ף��� | B�� | ƽ���Ӧ���ȣ��ף��� | ||
| C�� | 500���¸÷�Ӧƽ�ⳣ����K=3��102 | D�� | ��a��0����0.9��b��l |
���� A����ʼ��Ӧ���ʺ���ֵ�Ũ�ȴ�С�йأ�
B����Ӧ����ЧӦ�ͷ�Ӧ���е�ת�����Լ�����IJ��������йأ�
C����������ʽ���K����������ƽ��Ũ��ϵ������֮���ͷ�Ӧ��ƽ��Ũ��ϵ������֮���ı�ֵ�����㷴Ӧ��ƽ�ⳣ����
D���ҡ����г�ʼ��Ӧ����ͬ��ƽ����Ӧ����ֵ����������ȣ���ʱ���߽�����ƽ���ǵ�Ч�ģ��ݴ˻ش�
��� �⣺A���տ�ʼ��Ӧʱ�����и���ֵ�Ũ����ȣ����Կ�ʼ��Ӧ������ȣ���A����
B������һ��������ϵ�����ŷ�Ӧ�Ľ��У��ų�������ʹ����ϵ���¶����ߣ�����ƽ�������ƶ����������Ǻ�����ϵ�����Լ��൱�����ҵĻ����������ƶ��ˣ���ƽ���Ӧ���ȣ��ף��ң���B����
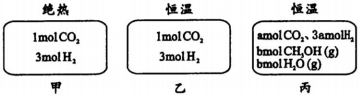
C���������̼��ת������xmol��CO2��g��+3H2��g��?CH3OH��g��ʮH2O��g��
��ʼ���ʵ�����1 3 0 0
�仯����x 3x x x
ƽ������1-x 3-3x x x
$\frac{1-x+3-3x+x+x}{4}$=0.55����ã�x=0.9������ƽ�ⳣ��K=$\frac{\frac{0.9}{10}��\frac{0.9}{10}}{\frac{1-0.9}{10}����\frac{3-3��0.9}{10}��^{3}}$=3��104����C����
D���ҡ����г�ʼ��Ӧ����ͬ��ƽ����Ӧ����ֵ����������ȣ���ʱ���߽�����ƽ���ǵ�Ч�ģ�����C�ļ��㣬ƽ��ʱ�״������ʵ�����0.9mol������0.9��b��l����D��ȷ��
��ѡD��
���� �����漰��ѧƽ��Ľ����Լ�Ӱ�췴Ӧ���ʵ����غ͵�Чƽ����й�֪ʶ�������ۺ�֪ʶ�Ŀ��飬�ѶȲ���


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Al3+��OH-��Cl- | B�� | H+��Mg2+��NO3-��SiO32- | ||
| C�� | Fe3+��NH4+��SCN-��F- | D�� | Na+��Cu2+��NO3-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 |  |  | 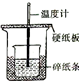 |
| A������п��ϡ���ᷴӦ������ | B������ͭпԭ��� | C����������к͵ζ�ʵ�� | D���ⶨ�к��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��A��B��C��D��E��F��G��W����ԭ���������������Ԫ�أ�ԭ��������С��30����Aԭ�ӵĺ������������Ӳ�����ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�E��Fͬ���壬G��Wͬ����ͬ����ԭ���������2����ش��������⣺
��A��B��C��D��E��F��G��W����ԭ���������������Ԫ�أ�ԭ��������С��30����Aԭ�ӵĺ������������Ӳ�����ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�E��Fͬ���壬G��Wͬ����ͬ����ԭ���������2����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ڢ�A��ĵ����ס��飨As����Ԫ���ڻ������г����ֳ���������̬�����ڢ�A��Ԫ�صĻ��������о�����������������Ҫ��;��
�ڢ�A��ĵ����ס��飨As����Ԫ���ڻ������г����ֳ���������̬�����ڢ�A��Ԫ�صĻ��������о�����������������Ҫ��;��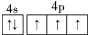 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Y | U | |||
| X | V | W |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 90% | B�� | 80% | C�� | 70% | D�� | 60% |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com