
c(H+)c(
| ||
c(H
|
c(H+)c(
| ||
c(H
|


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
| A、同一主族元素气态氢化物从上到下,其沸点逐渐升高 |
| B、非金属单质中一定存在共价键,离子化合物中可能存在共价键 |
| C、非极性键不可能存在于离子化合物中,由非金属元素组成的化合物中一定不存在离子键 |
| D、含有阴离子的物质一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、485.5 kJ/mol |
| B、610 kJ/mol |
| C、917 kJ/mol |
| D、1 220 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NH4HSO4溶液中逐滴加入NaOH溶液至中性,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) |
| B、等物质的量浓度的Na2CO3,NaHCO3混合溶液中c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C、已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中c(Na+)-c(F-)<c(K+)-c(CH3COO-) |
| D、在0.1mol/L 的Na2S溶液中 c(H+)+c(HS-)+c(H2S)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=6的由醋酸与醋酸钠组成的混合溶液中:c(Na+)>c(CH3COO-) |
| B、将Cl2通入过量KOH溶液中:c(ClO-)+c(Cl-)=c(K+) |
| C、0.1mol?L-1的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D、室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
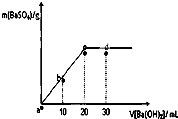 常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )| A、硫酸溶液的体积为20 mL |
| B、b时刻溶液中硫酸根离子浓度约为0.125 mol?L-1 |
| C、d时刻溶液的pH为13 |
| D、溶液的导电能力:c<d<b<a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com