
【题目】科学家在一100 ℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键)。下列说法正确的是
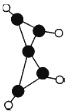
A. X既能使溴的四氯化碳溶液褪色,又能使酸性KMnO4溶液褪色
B. X是一种常温下能稳定存在的液态烃
C. X和l,3-丁二烯类似,能与Br2发生l,2-加成和1,4-加成
D. 充分燃烧等质量的X和甲烷,X消耗氧气较多
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列生活中常见物质与化学式相对应的是
A. 明矾:KAl(SO4)2 B. 水玻璃:CaSiO3
C. 酒精——C2H5OH D. 小苏打:Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:醛(或酮)在一定条件下(稀NaOH溶液中)可以两分子加成得到β-羟基醛(或酮),后者微热脱水生成α、β不饱和醛(或酮)。
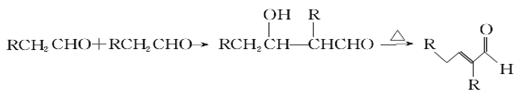
聚合物F的合成路线图如下:
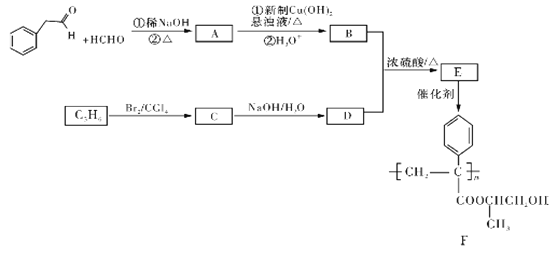
请据此回答:
(1)A中含氧官能团名称是_________。
(2)E→F的反应类型是____________。
(3)写出下列反应的化学方程式:
A→B的反应①__________________________;
C→D:____________________________;
(4)已知同一个碳原子上连两个碳碳双键的结构不稳定,如果C与NaOH的醇溶液反应,则生成的有机物的结构简式为_______________。
(5)G物质与![]() 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比![]() 大14,则符合下列条件的G的同分异构体有________种。
大14,则符合下列条件的G的同分异构体有________种。
① 分子中含有苯环,且苯环上有两个取代基
② 遇氯化铁溶液变紫色
③ 能与溴水发生加成反应
(6)参照上述合成路线,设计一条由甲醛、丙醛和甲醇为有机原料(除溶剂外不得使用其它有机物)合成有机玻璃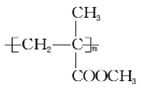 的合成路线。____________
的合成路线。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下对核外电子运动状况的描述正确的是( )
A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转
B.能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动
C.能层序数越大,s原子轨道的半径越大
D.在同一能级上运动的电子,其运动状态肯定不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下流程中a、b、c、d、e、f是六种有机物,其中a是烃类,其余是烃的衍生物。下列有关说法正确的是
![]()
A. 若a的相对分子质量是42,则d是乙醛
B. 若d的相对分子质量是44,则a是乙炔
C. 若a为苯乙烯(C6H5-CH=CH2),则f的分子式是C16H32O2
D. 若a为单烯烃,则d与f的最简式可能相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 甲酸溶液导电性比乙酸溶液导电性强,说明乙酸是弱酸
B. 硫酸钾溶于水能导电,所以硫酸钾是电解质
C. 强电解质一定是含有离子键,弱电解质中一定含弱极性共价键
D. 固态磷酸是电解质,所以磷酸在熔融状态下和水溶液中都能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾。
(1)SO2和O2反应制取SO3的反应原理为2SO2(g)+O2(g) ![]() 2SO3(g),在一密闭容器中一定时间内达到平衡。
2SO3(g),在一密闭容器中一定时间内达到平衡。
①该反应的平衡常数表达式为K=________。
②该反应达到平衡状态的标志是________。
A.v(SO2)=v(SO3)
B.混合物的平均相对分子质量不变
C.混合气体质量不变
D.各组分的体积分数不变
(2)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。

① B电极的电极反应式_______________________________________。
②溶液中H+的移动方向由________极到________极(用A、B表示);
(3)测定绿矾产品中含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL溶液
b.量取25 mL待测液于锥形瓶中
c.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积40 mL
根据上述步骤回答下列问题:
①滴定时发生反应的离子方程式为(完成并配平离子反应方程式)。
________Fe2++________MnO![]() +________===________Fe3++________Mn2++________
+________===________Fe3++________Mn2++________
② 用硫酸酸化的KMnO4滴定终点的标志是
___________________________________
___________________________________。
③计算上述产品中FeSO4·7H2O的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com