
【题目】亚硝酸钠是重要的防腐剂.某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠.(夹持装置和A中加热装置已略,气密性已检验),查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2﹣可将MnO4﹣还原为Mn2+ .
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;③从C中取少量固体,检验是否是亚硝酸钠.
回答下列问题:
(1)装置中仪器a的名称为;D装置的作用是 .
(2)A中反应的化学方程式是;C中反应生成NaNO2的化学方程式是 .
(3)检验C中产物有亚硝酸钠的正确操作是 .
a.取少量生成物溶于水充分振荡,滴加酚酞试液,若溶液变红,则含有NaNO2 .
b.取少量生成物溶于稀硫酸,若产生无色气体并在液体上方变为红棕色,则含有NaNO2 .
(4)经检验C产物中亚硝酸钠含量较少.
①.甲同学认为C中产物不仅有亚硝酸钠,还可能有其它固体物质.为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂应是(写名称).
②.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 .
【答案】
(1)分液漏斗;除去未反应的NO,防止污染空气
(2)C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2
CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2
(3)b
(4)碱石灰;打开弹簧夹,通入N2一段时间
【解析】解:(1)a名称是分液漏斗;NO有毒不能直接排空,NO和酸性高锰酸钾溶液反应生成硝酸根离子和锰离子,从而除去NO,所以答案是:分液漏斗;除去未反应的NO,防止污染空气;(2)C和HNO3(浓)发生反应生成CO2、NO2、H2O,反应方程式为C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;NO和Na2O2发生反应生成NaNO2 , 反应方程式为 2NO+Na2O2=2NaNO2 ,
CO2↑+4NO2↑+2H2O;NO和Na2O2发生反应生成NaNO2 , 反应方程式为 2NO+Na2O2=2NaNO2 ,
所以答案是:C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2;(3)a.A中生成二氧化碳,二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠溶液也呈碱性,B中出来的气体中还含有水蒸气能和C中的过氧化钠反应生成NaOH而呈碱性,所以不能根据其水溶液判断含有亚硝酸钠,故a错误;
CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2;(3)a.A中生成二氧化碳,二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠溶液也呈碱性,B中出来的气体中还含有水蒸气能和C中的过氧化钠反应生成NaOH而呈碱性,所以不能根据其水溶液判断含有亚硝酸钠,故a错误;
b.亚硝酸钠能和稀硫酸反应生成无色气体NO,NO不稳定易被氧气氧化生成红棕色气体二氧化氮,该实验现象说明含有亚硝酸钠,故b正确;
故选:b;(4)①从B装置中出来的气体中含有NO、二氧化碳和水蒸气,这几种物质都能和过氧化钠反应,要使C中只有NO和过氧化钠反应,则BC装置间的E装置应该能吸收水蒸气和二氧化碳,使用的药品是碱石灰,
所以答案是:碱石灰;
②要排除空气防止发生反应,应该先通入一段时间的氮气,所以答案是:打开弹簧夹,通入N2一段时间.


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
【题目】CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
(1)Cu2+基态的电子排布式可表示为;
(2)SO42﹣的空间构型为(用文字描述);中心原子采用的轨道杂化方式是;写出一种与SO42﹣互为等电子体的分子的化学式:;
(3)向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4]2﹣ . 不考虑空间构型,[Cu(OH)4]2﹣的结构可用示意图表示为;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 .
(5)CuS比CuO的熔点(填高或低),原因是 .
(6)闪锌矿的主要成分ZnS,晶体结构如图所示,其晶胞边长为540.0pm,密度为(列式并计算),a位置S2﹣离子与b位置Zn2+离化学﹣选修5:有机化学基础子之间的距离为pm(列式表示). 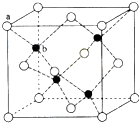
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出) 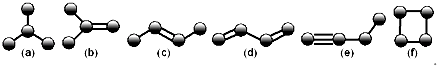
(1)写出有机物(a)的系统命名法的名称;
(2)有机物(a)有一种同分异构体,试写出其结构简式;
(3)上述有机物中与(c)互为同分异构体的是;(填代号)
(4)任写一种与(e)互为同系物的有机物的结构简式;
(5)上述有机物中不能与溴水反应使其褪色的有 . (填代号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是( ) 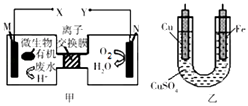
A.M电极反应式:(C6H10O5)n+7nH2O﹣24ne﹣═6nCO2↑+24nH+
B.铜电极应与X相连接
C.质子透过离子交换膜由右向左移动
D.当N电极消耗0.2 mol气体时,则铁电极增重16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设C+CO22CO;△H>0,反应速率为v1;N2+3H22NH3;△H<0,反应速率为v2 , 对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.NH4HCO3溶于过量的浓KOH溶液中并加热:NH4++HCO3﹣+2OH﹣=CO32﹣+NH3↑+2H2O
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42﹣沉淀完全:2Al3++3SO42﹣+3Ba2++6OH ﹣=2 Al(OH)3↓+3BaSO4↓
C.向FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl﹣
D.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3﹣═3Fe3++NO↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的化合物的说法中,正确的是( )
A.Na2CO3和NaHCO3均能与盐酸和NaOH溶液反应
B.NaHCO3固体中混有的Na2CO3可用加热的方法除去
C.Na2O2和Na2O中阴阳离子个数比均为1:2
D.分别向Na2O2和Na2O与水反应后的溶液中立即滴入酚酞溶液,现象相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 下列说法不正确的是( )
下列说法不正确的是( )
A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性
B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关
C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化
D.燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com