
下列物质中:
(1)互为同分异构体的有 (2)互为同素异形体的有
(3)属于同位素的有 (4)属于同一种物质的有 。(填序号)
①氯;②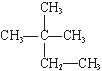 ;③白磷;④氯气;
;③白磷;④氯气;
⑤ ;⑥
;⑥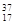 Cl;⑦
Cl;⑦ Cl;⑧红磷
Cl;⑧红磷
②⑤;③⑧;⑥⑦;①④
解析试题分析:(1)分子式相同结构不同的化合物互为同分异构体,所以互为同分异构体的是②和⑤,即答案选②⑤。
(2)由同一种元素形成的不同单质,互为同素异形体,则白磷和红磷互为同素异形体,答案选③⑧。
(3)质子数相同,中子数不同的同一种元素的不同核素互称为同位素,所以互为同位素的是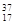 Cl和
Cl和 Cl,答案选⑥⑦。
Cl,答案选⑥⑦。
(4)结构和性质完全相同的是同一种物质,所以属于同一种物质的是①④,答案选①④。
考点:考查同系物、同分异构体、同位素以及同一种物质的判断
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。该题的关键是明确同系物、同分异构体、同位素以及同一种物质的含义、判断依据,然后结合题意灵活运用即可。


科目:高中化学 来源: 题型:填空题
(15分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下: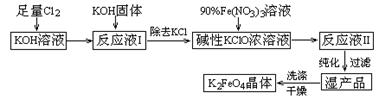
已知:① 2KOH + Cl2 =" KCl" + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 =" 5KCl" + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH = 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4可作为新型多功能水处理剂的原因 ;
(4)与MnO2 — Zn电池类似,K2FeO4 — Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为________,该电池总反应的离子方程式为_____。
(5)在“反应液I ”中加KOH固体的目的是① ,② ;
(6)从“反应液II ”中分离出K2FeO4后,副产品是 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图为一“铁链”图案,小明在图案上由左到右分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号。
请回答下列问题:
(1)请将分类依据代号填入相应的括号内
( )两种物质都不是电解质
( )两种物质都是钠的化合物
( )两种物质都是氧化物
( )两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入
1 mol·L-1的图中一种化合物的水溶液,可制得一种红褐色胶体。
①反应的化学方程式为:________________________________________________。
②如何用较简单的方法判断胶体是否制备成功?
___________________________________________________________
③向该胶体中逐滴加入盐酸,会出现一系列变化:
a.先出现红褐色沉淀,原因是___________________________________________
b.随后红褐色沉淀溶解,此反应的离子方程式是____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
无机化合物可根据其组成和性质进行分类:
(1)上述所示的物质分类方法名称是 。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②、③和⑥后面。(每空填写一个化学式即可)
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(11分)Ⅰ.分类法是化学学习的一种十分有效的方法,它可以使我们从不同角度对同一知识做更加深入的了解,人们根据不同的标准,即使同一物质也可能被划在不同的类别中。现有如下物质①MgCl2②HCl ③SO2 ④ NO2 ⑤K2CO3 ⑥ Cl2 ⑦CaO ⑧ NaOH
请根据下列标准,对上述物质进行分类:
(1)既含离子键又含共价键的物质是 (填代号,下同)。
(2)只含共价键且为非电解质的是 。
(3)含有共价键的化合物是 。
Ⅱ.向某恒容的密闭容器中加入A、B、C三种气体,如图所示是一定条件下三种气体的物质的量随时间的变化情况。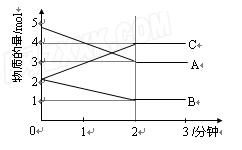
(1)写出该密闭容器发生反应的化学方程式为 。
(2)2分钟后A、B、C各物质的量不再随时间的
变化而变化,其原因是____ 。
(3)下列情况能说明该反应达到化学反应限度的是 。
A.该容器的压强不再发生变化;
B.单位时间内生成A的物质的量与生成C的物质的量相同;
C.该容器中气体的密度不再改变;
D.容器中A的物质的量与C的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列对各组离子或物质是否能够大量共存解释正确的是 ( )
| A | 常温常压下NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体,CO2为酸性气体,二者反应生成(NH4)2CO3 |
| B | c(OH-)=1×10-13mol/L溶液中,Fe2+、NO3-、SO42-、Na+ | 不能共存 | 发生反应Fe2++NO3-+4H+=3Fe3++NO+2H2O |
| C | 溶液中: K+、Cu2+、Cl-、NH3?H2O | 不能共存 | 发生反应Cu2++2OH-=Cu(OH)2 |
| D | 溶液中Al3+、Na+、SO42-、HCO3- | 可以共存 | 不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关叙述中正确的是
| A.难溶于水的电解质一定是弱电解质 |
| B.强电解质在水溶液中的电离过程是不可逆的 |
| C.易溶于水的电解质一定是强电解质 |
| D.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是
| A.NH4+、K+、Cl-、OH- | B.H+、Fe2+、MnO4-、Cl- |
| C.Ba2+、Na+、NO3-、SO42- | D.Na+、H+、CO32-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com