
【题目】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构,为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为_____,能证明凯库勒观点错误的实验现象是_____。
(2)装置B的作用是_________。
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为_______mL。(空气的平均相对分子质量为29)
(4)已知乳酸的结构简式为:![]() 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:______。
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:______。
【答案】![]() +Br2
+Br2![]() +HBr C中产生喷泉现象 除去未反应的溴蒸气和苯蒸气 450 CH3CH(OH)COOH+NaOH=CH3CH(OH)COONa+H2O
+HBr C中产生喷泉现象 除去未反应的溴蒸气和苯蒸气 450 CH3CH(OH)COOH+NaOH=CH3CH(OH)COONa+H2O
【解析】
(1)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,苯分子里的氢原子被溴原子所代替,方程式为: ![]() +Br2
+Br2![]() +HBr,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
+HBr,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
(2)因为反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验H+和Br-;
(3)烧瓶中混合气体对H2的相对密度为37.9,故烧瓶中混合气体的平均分子量为37.9×2=75.8,设HBr的体积为x,空气的体积为y,则: ,计算得出:x=450mL,y=50mL,故进入烧瓶中的水的体积为x=450mL;
,计算得出:x=450mL,y=50mL,故进入烧瓶中的水的体积为x=450mL;
(4)乳酸跟氢氧化钠溶液反应的化学方程式为CH3CH(OH)COOH+NaOH=CH3CH(OH)COONa+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硒及其化合物在生产、生活中有着广泛的应用,掺杂硒的纳米氧化亚铜常用作光敏材料、电解锰行业催化剂等。
(1)酸性溶液中Na2SO3将H2SeO3和H2SeO4还原为晒单质的反应如下:
H2SeO3(aq)+2SO2(g)+H2O(l)=Se(s)+2H2SO4(aq) △H1
2H2SeO4(aq)+Se(s)+H2O(l)=3H2SO4(aq) △H2
H2SeO4(aq)+2SO2(g)+2H2O(l)=Se(s)+3H2SO4(aq) △H3
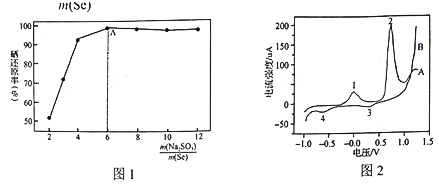
实验中控制其他条件不变(盐酸浓度等),![]() 与硒还原率关系如图1。在A点之前,随着
与硒还原率关系如图1。在A点之前,随着![]() 的增加,Se的还原率不断升高的原因是_____________。
的增加,Se的还原率不断升高的原因是_____________。
(2)向Na2SeO3溶液中加入适量的AgNO3溶液,得到Ag2Se纳米晶体,同时产生N2。该反应的离子方程式为 ______。
(3)制 PbSe 纳米管时还产生了副产物PbSeO3。己知:Ksp(PbSeO3)=3×l0-12, Ksp(PbSe)= 3×l0-38。为了除去PbSe中混有的PbSeO3,可以采取的措施是______。
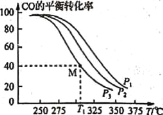
(4)实验室测得碱性条件下PbSe纳米管在电极表面的氧化还原行为,结果如图2所示。其中一条曲线上的峰表示氧化过程,另一条曲线上的峰表示还原过程。整个过程共发生如下变化:Pb(OH)2—PbO2;Pb(OH)2—Pb; PbSe—Se; PbO2→Pb(OH)2,各物质均难溶于水。峰1对应的电极反应式为:PbSe-2e-+2OH-=Pb(OH)2+Se;则峰2对应的电极反应式为 ______。
(5)掺杂硒的纳米Cu2O催化剂可用于工业上合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
①压强P1、P2、P3由小到大的顺序是 __________。
②T1 ℃时若向该容器中充入2.0 mol H2和2.0 mol CO发生上述反应,5 min后反应达到平衡(M点),则M点对应条件下反应的平衡常数为 ______。
(6)将CuCl水解再热分解可得到纳米Cu2O。CuCl 水解的反应为 CuCl(s) +H2O(1) ![]() CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)烧杯间填满碎泡沫塑料的作用是___________________________
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?_______(填“能”或“不能”), 其原因是____________________________。
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是___________________________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量________________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙烷和乙烯都能用来制取氯乙烷,且反应类型相同
B. 无水乙醇比医用酒精的消毒效果更好
C. 除去甲烷的乙烯可通过酸性高锰酸钾溶液洗气
D. 甲苯和乙苯都是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为2CH3OH+3O2===2CO2+4H2O。下列说法中不正确的是

A. 左边的电极为电池的负极,a处通入的是甲醇
B. 每消耗3.2 g氧气转移的电子为0.4 mol
C. 电池负极的反应式为CH3OH+H2O6e===CO2+6H+
D. 电池的正极反应式为O2+2H2O+4e===4OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种变化是因为构成原电池的是( )
A.在空气中金属铝表面迅速氧化形成保护层
B.金属表面涂漆以阻止金属被氧化
C.红热的铁丝与水接触铁表面形成黑色物质
D.铁与稀硫酸反应时,加人少量硫酸铜溶液后可使反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油和淀粉或纤维素为原料均可制得乙酸乙酯,转化关系如下图:
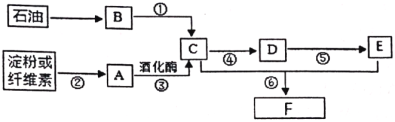
其中气体B在标况下的密度为:1.25 g/L。请回答:
(1)B中官能团的名称是________。
(2)A的分子式是________。
(3)反应④的化学方程式为________。
(4)下列说法正确的是________。
A.反应②⑤⑥属于取代反应
B.物质F的结构简式为CH3CH2OOCCH3
C.B和E可在一定条件下直接合成F,该方法符合绿色化学理念
D.可用新制氢氧化铜鉴别C、D、E三种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl)试剂_______,离子方程式:____________________________________。
(2)CO2(HCl)试剂___________,离子方程式:__________________________________。
(3)O2(CO2)试剂__________,离子方程式:____________________________________。
(4)SO42-(CO32-)试剂_______,离子方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。现有Ca(OH)2溶液,向其溶液中逐渐通入CO2。则下列四个图中,能比较准确地反映出溶液的导电能力和通入CO2气体量的关系的是(x轴表示CO2通入的量,y轴表示导电能力)
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com