
����Ŀ����A��B��C��D����Ԫ�أ�����AԪ����1826��һλ���������ѧ�ҷ��ֵģ������о���ˮ����ʱ��ʣ��ĸ�����(��±)��ͨ������������Һ����ɫ�������һ����ȡ�ɵú���ɫҺ�壬�д̼�����ζ��B��C��D�ĺ�����Ӳ���������3����Dԭ�Ӻ��ڵ����������õ���Cԭ�Ӻ�����������2���������ǵ�������������ȣ�Dԭ�ӵ����ڲ��������Bԭ�Ӻ����������2�����ش��������⣺
��1������Ԫ�طֱ�ΪA��_____��B��____��C��_____��D��_____��
��2��Aԭ�ӵĵ����Ų�ʽΪ________��Dԭ�ӵ�ԭ�ӽṹʾ��ͼΪ______��
��3��д��������Ԫ����ɵĵ��ʺͻ�������������ɳ�����������ѧ����ʽ________��_______��
���𰸡�Br(��) H(��) O(��) S(��) 1s22s22p63s23p63d104s24p5��[Ar]3d104s24p5 ![]() 2H2S��O2===2S����2H2O H2S��Br2===S����2HBr
2H2S��O2===2S����2H2O H2S��Br2===S����2HBr
��������
AԪ����1826��һλ���������ѧ�ҷ��ֵģ������о���ˮ����ʱ��ʣ��ĸ�����(��±)��ͨ������������Һ����ɫ�������һ����ȡ�ɵú���ɫҺ�壬�д̼�����ζ������֪��ΪBrԪ�أ�
Dԭ�Ӻ��ڵ����������õ���Cԭ�Ӻ�����������2���������ǵ�������������ȣ����Ƴ�CΪOԪ�أ�DΪSԪ�أ�
Dԭ�ӵ����ڲ��������Bԭ�Ӻ����������2������BԪ��ΪH���ݴ˷�������
��1������Ԫ�طֱ�ΪAΪBr(��)��BΪH(��)��CΪO(��)��DΪS(��)��
��2��AΪBr����ԭ������Ϊ26�����ݵ����Ų����ɿ�֪��������Ų�ʽΪ1s22s22p63s23p63d104s24p5��[Ar]3d104s24p5��DΪS����ԭ������Ϊ16��ԭ�ӽṹʾ��ͼΪ![]() ���ʴ�Ϊ��1s22s22p63s23p63d104s24p5��
���ʴ�Ϊ��1s22s22p63s23p63d104s24p5��![]() ��
��
��3�����ݷǽ������ʵ������Թ��ɿ�֪�����ʺͻ�������������ɵij���ΪS����������������Ծ�����S���ʻ�ѧ����ʽΪ��2H2S��O2===2S����2H2O��H2S��Br2===S����2HBr��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ij�л������ʽΪC4H10O���������Ʒ�Ӧ�ų����������������칹������ͬ���칹����ĿΪ5
B.��ϩ�ͱ�����ʹ��ˮ��ɫ����ԭ����ͬ
C.��ˮ�ɼ����Ҵ�����������
D.��Na��Ӧ�ľ��ҳ̶ȣ�CH3COOH>CH3CH2OH>H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H��һ���л��������м��塣ʵ�����ɷ��㻯����A�Ʊ�H��һ�ֺϳ�·�����£�
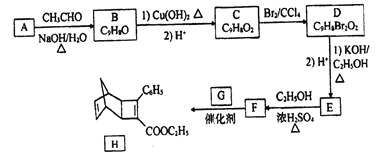
��֪����RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
��![]()
�ش���������:
(1) E�Ľṹ��ʽΪ_______��
(2) E����F�ķ�Ӧ����Ϊ_______��
(3) 1mol������H������_______molH2�����ӳɷ�Ӧ��
(4)GΪ�ױ���ͬ���칹�壬��F����H�Ļ�ѧ����ʽΪ______��
(5)���㻯����X��Fͬ���칹�壬X���뱥��̼�����Ʒ�Ӧ�ų�CO2����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�����⣬�������֮Ϊ6:2:1:1��д��1�ַ���Ҫ���X�Ľṹ��ʽ_____��
(6)д���û������2-��ȲΪԭ���Ʊ�������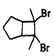 �ĺϳ�·��(�����Լ���ѡ)_____��
�ĺϳ�·��(�����Լ���ѡ)_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������η���E��ֱ���η���G��Ӧ�����������η���L��ֱ���η���M(���E��Ԫ�ص�ԭ��������С��10�����G��Ԫ��Ϊ��������Ԫ��)�ķ�Ӧ������ͼ��ʾ���������ж���ȷ����( )

A.���³�ѹ�£�L��һ��Һ̬�л���
B.E��һ�ֺ��зǼ��Լ��ķ���
C.G��ʹ�������ɫ������ɫ
D.�÷�Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ��Ϊͬ���칹����ǣ� ��
��Ϊͬ���칹����ǣ� ��
A.OHCCH2CH2CHOB.CH3CH2OCH2CH2OH
C.CH3CH=CHCOOHD.HOCH2CH=CHCH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2��g����I2��g����H2��g����I2��s)�Լ�HI��g���������ߵ���ͼ��ʾ�������жϴ�����ǣ� ��
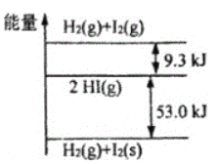
A.1molH2��g����1molI2��g���������ܺ���2molHI��g��������
B.I2��g����I2��s��+QkJ��Q>0��
C.H2��g��+I2��g����2HI��g��+9.3kJ
D.H2��g��+I2��s����2HI��g��+53.0kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��C(s)��O2(g)===CO2(g)����H1
CO2(g)��C(s)===2CO(g)�� ��H2
2CO(g)��O2(g)===2CO2(g)����H3
4Fe(s)��3O2(g)===2Fe2O3(s)�� ��H4
3CO(g)��Fe2O3(s)===3CO2(g)��2Fe(s)����H5
���й���������Ӧ�ʱ���ж���ȷ����
A. ��H1��0����H3��0B. ��H2��0����H4��0C. ��H1����H2����H3D. ��H3����H4����H5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ͭпԭ���ʾ��ͼ��ͼ2�У�x���ʾʵ��ʱ���������ĵ��ӵ����ʵ�����y���ʾ�� ��

A. c(H+) B. V(H2) C. m(��Һ) D. m(Cu)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʪ����п�ĵ��Һ��ͬʱ����Cu��CuSO4��������CuCl������ȥCl-�����ͶԵ���Ӱ�죬��Ӧԭ�����£�
Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ��H1=akJ��mol-1
2Cu+(aq) ��H1=akJ��mol-1
Cl��(aq)+Cu+(aq)![]() CuCl(s) ��H2=bkJ��mol-1
CuCl(s) ��H2=bkJ��mol-1
ʵ���õ��ҺpH����Һ�в���c(Cl-)��Ӱ����ͼ��ʾ������˵����ȷ���ǣ� ��
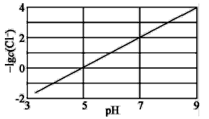
A.����ͭ���ʵ�����������Cl-��ȥ��
B.��ҺpHԽ��Ksp(CuCl)����
C.��Ӧ�ﵽƽ�������c(Cu2+)��c(Cl-)��С
D.![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl-(aq)
Cu2+(aq)+Cl-(aq)![]() CuCl(s)����H=(a+2b)kJ��mol-1
CuCl(s)����H=(a+2b)kJ��mol-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com