
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。

请回答下列问题:
(1)葡萄糖的结构简式为__________,B分子中的官能团名称为_______。
(2)反应⑦中物质X的分子式为_________,反应⑧的类型为_________。
(3)反应③的化学方程式为_______。
(4)反应⑤的化学方程式为_________。反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是______。
(5)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为_____。
(6)检验反应①进行程度,需要的试剂有________。
A 新制的Cu(OH)2悬浊液 B 碘水
C NaOH溶液 D FeCl3溶液
(7)乙烯的同系物丙烯(CH2=CH-CH3)可以通过加聚反应生成高分子化合物,其结构简式是___________。
【答案】CH2OH(CHOH)4CHO 羧基 Br2 取代反应 2CH3CH2OH + 2O2![]() 2CH3CHO + 2H2O CH3CH2OH+ CH3COOH
2CH3CHO + 2H2O CH3CH2OH+ CH3COOH ![]() CH3COOCH2CH3 + H2O NaOH溶液 C4H6O4 ABC
CH3COOCH2CH3 + H2O NaOH溶液 C4H6O4 ABC ![]()
【解析】
CH3CH2OH在Cu催化剂条件下发生催化氧化生成A为CH3CHO,CH3CHO进一步氧化生成B为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成C为CH3COOC2H5,乙醇发生消去反应生成乙烯,乙烯与Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NC-CH2CH2-CN,(5)中D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则分子中![]()
、![]() 、
、![]() ,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH,以此分析。
,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH,以此分析。
CH3CH2OH在Cu催化剂条件下发生催化氧化生成A为CH3CHO,CH3CHO进一步氧化生成B为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成C为CH3COOC2H5,乙醇发生消去反应生成乙烯,乙烯与Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NC-CH2CH2-CN,(5)中D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则分子中![]()
、![]() 、
、![]() ,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH。
,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH。
(1) 葡萄糖的结构简式为CH2OH(CHOH)4CHO,分子中的官能团为羧基,故答案为:CH2OH(CHOH)4CHO;羧基;
(2)反应⑦中物质X的分子式为Br2,反应⑧的类型为取代反应,故答案为:Br2;取代反应;
(3) 反应③的化学方程式为2CH3CH2OH + 2O2![]() 2CH3CHO + 2H2O,故答案为:2CH3CH2OH + 2O2
2CH3CHO + 2H2O,故答案为:2CH3CH2OH + 2O2![]() 2CH3CHO + 2H2O;
2CH3CHO + 2H2O;
(4)反应⑤的化学方程式为CH3CH2OH+ CH3COOH ![]() CH3COOCH2CH3 + H2O,反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液,故答案为:CH3CH2OH+ CH3COOH
CH3COOCH2CH3 + H2O,反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液,故答案为:CH3CH2OH+ CH3COOH ![]() CH3COOCH2CH3 + H2O;NaOH溶液;
CH3COOCH2CH3 + H2O;NaOH溶液;
(5)由上述分析可知,D的分子式为:C4H6O4,故答案为:C4H6O4;
(6)反应①是淀粉水解生成葡萄糖,葡萄糖中含有醛基,检验进行程度的实验方案:取反应①的溶液于试管中,用NaOH溶液调节溶液至碱性,再加入新制的Cu(OH)2悬浊液,加热一段时间,若有砖红色沉淀,则证明反应①已发生;另取反应①的溶液,加入碘水,变蓝,说明还有淀粉,否则没有,故答案为:ABC。
(7) 乙烯的同系物丙烯(CH2=CH-CH3)可以通过加聚反应生成高分子化合物,其结构简式是![]() ,故答案为
,故答案为![]() 。
。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】现有HA、HB和H2C三种酸。室温下用0.1mol·L- 1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示。

(1)原HA中水电离出的c(H+)=________mol·L-1
(2)与曲线I上的c点对应的溶液中各离子浓度由大到小的顺序为________;b点对应的溶液中c(HB)____c(B-)(填“>”“<”或“=”)。
(3)已知常温下向0.1mol·L-1的NaHC溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为_______________。
②若在此溶液中能检测到H2C分子,则此溶液中c(C2-)________c(H2C)(填“>”“<”或“=”)。
③若H2C的一级电离为H2C=H++HC-,常温下0.1mol·L-1H2C溶液中的c(H+)=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)________0.01mol·L-1(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CH3OH(g) +3/2O2(g)=CO2(g)+2H2O(g) △H=-akJ·mol一1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-bkJ·mol一1
③CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H=-ckJ·mol一1
则下列叙述正确的是( )
A. 由上述热化学方程式可知b>c
B. 甲烷的燃烧热为bkJ/mol
C. 2CH3OH(g)=2CH4(g) +O2(g) △H=2(b一a)KJ mol一1
D. 当甲醇和甲烷物质的量之比为1:2时,其完全燃烧生成CO2和H2O(1)时,放出的热量为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 对于2NO2(g)![]() N2O4(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅
N2O4(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅
B. 化学平衡正向移动,反应物的转化率一定增大
C. 往平衡体系FeCl3+3KSCN![]() Fe(SCN)3+3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅
Fe(SCN)3+3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅
D. C(s)+CO2(g)![]() 2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO2)和CO2的平衡转化率均增大
2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO2)和CO2的平衡转化率均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是________。
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,则通入a气体的电极名称为_____,通入b气体的电极反应式为____。(质子交换膜只允许H+通过)
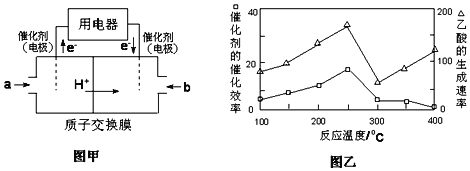
(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在__左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为___________。
(4)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx气体反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx气体,则x值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、X、Y和Z的原子序数依次增大,RZ3溶于水生成一种具有漂白性的物质,生成的另一种物质的分子模型如图A所示。X和Y的单质按一定比例混合后恰好能完全溶于足量水中,在其水溶液中缓慢通入CO2气体,沉淀质量(m)与CO2的体积(V)的关系如图B所示。

下列说法一定正确的是( )
A. Y一定位于第三周期第ⅢA族B. 原子半径:X>Y>Z
C. Z与X、Y均形成离子化合物D. R和Z的氧化物对应的水化物都是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱法又称联合制碱法,是我国化学工程专家侯德榜于1943年发明的。此方法具有食盐利用率高、对环境的污染少、生产成本低等优点。其制备中涉及如下两个反应:NaC1+H2O+CO2+NH3===NaHCO3↓+NH4Cl、2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(1)基态氯原子的电子排布式为___,基态氮原子最高能级上电子自旋方向均相同,这是由____规则(原理)确定的,C、N、O三种元素第一电离能由大到小的顺序为____。
(2)H2O、CO2、NH3三种分子中,中心原子的杂化轨道类型为sp的是___,属于V形分子的是____。在常温常压下,1体积水可溶解700体积NH3、可溶解0.8体积CO2,试解释其原因:_____。
(3)要确定Na2CO3固体是晶体还是非晶体,最可靠的方法是___,下列事实不能支持Na2CO3的晶体类型为离子晶体的是___(填字母)。
a.熔点为851℃ b.晶体中存在Na+、CO32-
c.可溶于水 d.晶体中存在离子键,共价键
(4)钠、氧两元素可形成两种常见化合物,其中一种的晶胞如下图所示(图中微粒表示相应的结构微粒),则该氧化物的化学式为___,若晶胞参数为d pm,晶胞的密度为![]() ,则阿伏加德罗常数NA=___(用含d、
,则阿伏加德罗常数NA=___(用含d、![]() 的代数式表示)。
的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应:2A(g)+2B(g)![]() C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是( )
C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是( )
A. 移走少量C B. 扩大容积,减小压强
C. 缩小容积,增大压强 D. 容积不变,充入“惰”气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是主族的三种非金属元素,它们在周期表中的位置如图所示:
X | ||
Y | ||
Z |
(1) Y元素的名称是_________。
(2) X元素的原子结构示意图是_________;X单质和氢气反应,生成的氢化物的化学式______。
(3)X、Y、Z的原子半径从大到小排列_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com