
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol?L﹣1 CH3COOH溶液中加入少量水,溶液中 ![]() 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中 ![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中 ![]() >1
>1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3 , 溶液中 ![]() 不变
不变
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):
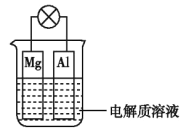
(1)电解质溶液为稀硫酸时,灯泡______ (填“亮”或“不亮”,填“亮”做 a 题,填“不亮”做 b题)。
a.若灯泡亮, Al 电极上发生的反应为______。
b.若灯泡不亮, 其理由为______。
(2)电解质溶液为 NaOH 溶液时,灯泡______ (填“亮”或“不亮”,填“亮”做 a 题,填“不亮”做 b 题)。
a.若灯泡亮, Al 电极上发生的反应为______。
b.若灯泡不亮, 其理由为______。
Ⅱ. CH4 既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的电子式为______。
(2)以 CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理下图所示,则通入 a 气体的电极名称为______, 通入 b 气体的电极反应式______。(质子交换膜只允许 H+通过)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CCl4和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物。同学们对此有下列一些“理解”,你认为其中 不正确的是
A. 纳米级金刚石属于胶体 B. 制造过程中元素种类没有改变
C. CCl4是一种化合物 D. 这个反应是置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题:
(1)两种物质都是电解质的是 (填分类标准代号,下同),两种物质都是氧化物的是
(2)分类标准代号A表示 (多项选择)
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某相邻两种物质间能发生反应且有离子反应,写出该反应的离子方程式为:
(4)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热呈红褐色,得到的分散系称为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途.回答下列问题:
(1)画出砷的原子结构示意图 .
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫.写出发生反应的化学方程式 . 该反应需要在加压下进行,原因是 .
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s)△H1
H2(g)+2O2(g)=H3AsO4(s)△H1
H2(g)+ ![]() O2(g)=H2O(l)△H2
O2(g)=H2O(l)△H2
2As(s)+ ![]() O2(g)=As2O5(s)△H3
O2(g)=As2O5(s)△H3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的△H= .
(4)298K时,将20mL 3x molL﹣1 Na3AsO3、20mL 3x molL﹣1 I2和20mL NaOH溶液混合,发生反应:AsO33﹣(aq)+I2(aq)+2OH﹣AsO43﹣(aq)+2I﹣(aq)+H2O(l).溶液中c(AsO43﹣)与反应时间(t)的关系如图所示.
①下列可判断反应达到平衡的是(填标号).
a.溶液的pH不再变化
b.v(I﹣)=2v(AsO33﹣)
c.c (AsO43﹣)/c (AsO33﹣)不再变化
d.c(I﹣)=y molL﹣1
②tm时,v正 v逆(填“大于”“小于”或“等于”).
③tm时v逆tn时v逆(填“大于”“小于”或“等于”),理由是 .
④若平衡时溶液的pH=14,则该反应的平衡常数K为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为实验室常用的实验装置,回答有关问题:

(1)写出标号仪器名称:①________;②__________。
(2)用高锰酸钾固体制氧气,应选用发生装置________(填“A”或“B”),装入药品前应先________,反应的化学方程式是________________________________________。若用过氧化氢溶液和二氧化锰制取氧气,二氧化锰起________作用。
(3)用块状石灰石制取二氧化碳时,②中应加入________,反应的化学方程式为________________________,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是________________(答出一点即可)。检验产生的气体是二氧化碳的方法是________________。
(4)实验室收集氢气可用________装置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如图: 
(1)“酸浸”过程中主要反应的离子方程式为:、 .
(2)“酸浸”时,提高浸出速率的具体措施有、 . (写出两个)
(3)“碱溶”的目的是 . 物质X的电子式为 . 该工艺设计中,过量X参与反应的离子方程式是: .
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com