
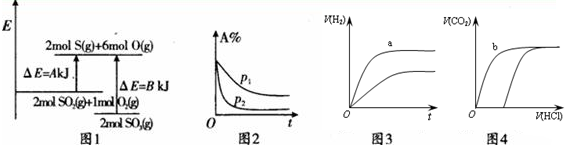
| A�� | ͼ1��ʾ��ѧ��Ӧ2S02��g��+O2��g��?2S03��g���������仯���÷�Ӧ�ġ�H=AһBkJ/mol | |
| B�� | ͼ2��ʾ������������ʱ����Ӧ2A��g��+B��g��?c��g��+D��g���ڲ�ͬѹǿ����ʱ��ı仯 | |
| C�� | ͼ3��ʾ�����Ũ�Ⱦ���ͬ��HCl��CH3COOH������Һ�У��ֱ����������п������H2�������ʱ��ı仯����a��ʾCH3COOH��Һ | |
| D�� | ͼ4��ʾ100 ml O��1 mol•L-Na2C03��NaHC03������Һ�У��ֱ���εμ�0.1 mol•L-1HCl������CO2 ���������������ı仯����b��ʾNaHCO3��Һ |
���� A����Ӧ�ʱ���ڲ��������ͷ�Ӧ������֮����ݷ�Ӧ�����������ش�
B��ѹǿԽ��Ӧ����Խ�죬����ѹǿ����ѧƽ�������ƶ�������A�ðٷֺ�����С��
C�������Ũ�Ⱦ���ͬ��HCl��CH3COOH������Һ�У��ֱ����������п��������ȫ���룬������Ũ�ȴ����ʿ죬���ߵ����ʵ���һ��������������һ���ࣻ
D��Na2C03��NaHC03������Һ�У��ֱ���εμ�HCl��̼���ƿ�ʼû������ų�������̼�����ƽ��žͷų����壬����̼Ԫ���غ�ȷ�����ղ���������̼������
��� �⣺A����Ӧ�ʱ���ڲ��������ͷ�Ӧ������֮���������������ڲ�����Է�Ӧ�ͷ����������Ը÷�Ӧ�ġ�H=AһBkJ/mol����A��ȷ��
B��ѹǿԽ��Ӧ����Խ�죬����P2����P1������ѹǿ����ѧƽ�������ƶ�������A�ðٷֺ�����С������ͼʾ��Ϣ����B��ȷ��
C�������Ũ�Ⱦ���ͬ��HCl��CH3COOH������Һ�У��ֱ����������п��������ȫ���룬������Ũ�ȴ����ʿ죬���Ƕ��ߵ����ʵ���һ��������п����������������������һ���࣬��ͼʾ��������C����
D��Na2C03��NaHC03������Һ�У��ֱ���εμ�HCl��̼���ƿ�ʼû������ų�������̼�����Ƽ���������žͷų����壬����̼Ԫ���غ㣬ȷ�����ղ���������̼������һ���ģ���ͼʾ��Ϣ�������D��ȷ��
��ѡC��
���� �����漰��ѧ��Ӧ����ЧӦ��������ʵĵ����Լ�̼���ơ�̼�����ƵĻ�ѧ���ʵȷ����֪ʶ�������ۺ�֪ʶ�Ŀ��飬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��AlCl3��Һ�еμӰ�ˮ���������ɫ�������ټ���NaHSO4����������ʧ | |
| B�� | Ũ��NaOH��Һ��������Ƥ���ϣ������ô���ˮ��ϴ����Ϳ�������ϡ������Һ | |
| C�� | AlCl3��Һ�м������NaF���壬�ٵμӰ�ˮ����������˵��[AlF6]3-���ѵ��� | |
| D�� | ����Cl-ʱ��Ϊ���ų�SO42-�ĸ��ţ����ȵμӹ�����Ba��NO3��2��Һ��ȡ�ϲ���Һ���ٵμ�AgNO3��Һ�����а�ɫ�����������ԭ��Һ����Cl-���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ij��ɫ��Һ�м��������ܲ�������H2�������Һ�д��ڴ���Na+��Ca2+��C1-��NO3- | |
| B�� | ˮ�������c��H+��=1��10-3mol•L-1��ˮ��Һ��Na+��CO32-��Cl-��K+ | |
| C�� | pH=1��ˮ��Һ��NH4+��Cl-��Mg2+��SO42- | |
| D�� | Al3+��HCO3-��I-��Ca2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
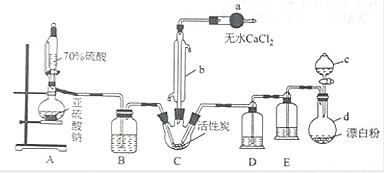 �Ȼ����Ǻϳ������ȣ�SO2Cl2���ij��÷�����ʵ���Һϳ������ȣ�SO2Cl2����ʵ��װ����ͼ��ʾ��
�Ȼ����Ǻϳ������ȣ�SO2Cl2���ij��÷�����ʵ���Һϳ������ȣ�SO2Cl2����ʵ��װ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  3-��-1��3-����ϩ 3-��-1��3-����ϩ | |
| B�� |  2-�ǻ����� 2-�ǻ����� | |
| C�� | CH3CH��C2H5��CH2CH2CH3 2-�һ����� | |
| D�� | CH3CH��CH3��CH2COOH 3-������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 1 mol•L-1 HCN��Һ��pHԼΪ3 | |
| B�� | HCN������ˮ | |
| C�� | 10 mL 1 mol•L-1 HCN��Һǡ����10 mL 1 mol•L-1NaOH��Һ��ȫ��Ӧ | |
| D�� | ����ͬ�����£�HCN��Һ�ĵ����Ա�ǿ����Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com