
���� ��������ʽ����A��B��C��ʼת��ƽ��ʱ������
��1������v=$\frac{��c}{��t}$�������ʣ�
��2����������ʽ��B��Ũ�ȣ�
��3������������������䣬�淴Ӧ���л�����������ʵ�����С������$\overline{M}$=$\frac{{m}_{��}}{{n}_{��}}$��֪��ƽ����Է������������������ݻ����䣬�ʻ�������ܶ�ʼ�ղ��䣮
��� �⣺��4molA�����2molB������2L�ܱ������л�ϲ���һ�������·�����Ӧ������2s����C��Ũ��Ϊ0.6mol/L�����������ʽ��
2A��g��+B��g��?2C��g��
��ʼ����mol/L����2 1 0
ת������mol/L����0.6 0.3 0.6
ƽ������mol/L����1.4 0.7 0.6
��1����������A��ʾ�ķ�Ӧ����v=$\frac{��c}{��t}$=$\frac{0.6mol/L}{2s}$=0.3 mol•L-1•s-1��
�ʴ�Ϊ��0.3 mol•L-1•s-1
��2����������ʽ֪2sʱ����B��Ũ�ȣ�0.7mol/L��
�ʴ�Ϊ��0.7mol/L��
��3������������������䣬�淴Ӧ���л�����������ʵ�����С������$\overline{M}$=$\frac{{m}_{��}}{{n}_{��}}$��֪��ƽ����Է������������������ݻ����䣬����ݦ�=$\frac{{m}_{��}}{V}$��֪����������ܶ�ʼ�ղ��䣻
�ʴ�Ϊ�������䣮
���� ���⿼���˻�ѧƽ���������ʽ�ķ��������Լ���ѧ��Ӧ���ʵļ��㡢Ũ�ȼ��㣬���ջ����ǹؼ�����Ŀ�ϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ��1-��ϩ | B�� | ������Ȳ | ||
| C�� | �������2-������ | D�� | �ױ����ұ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H2 | B�� | C3H4 | C�� | C3H8 | D�� | C4H6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
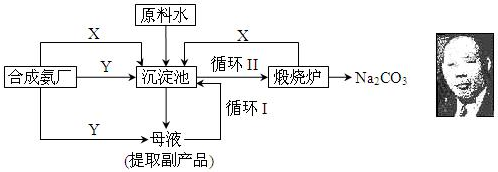
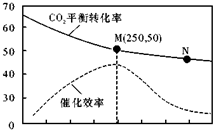 һ�������ºϳ���ϩ6H2��g��+2CO2��g��?CH2=CH2��g��+4H2O��g������֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������
һ�������ºϳ���ϩ6H2��g��+2CO2��g��?CH2=CH2��g��+4H2O��g������֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������| A�� | ������ϩ�����ʣ�v��M����v��N�� | |
| B�� | ƽ�ⳣ��KM��KN | |
| C�� | �������ܻ�Ӱ��CO2��ƽ��ת���� | |
| D�� | ��Ͷ�ϱ�n��H2����n��CO2��=3��1����ͼ��M��ʱ��CO2���������ԼΪ15.4% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
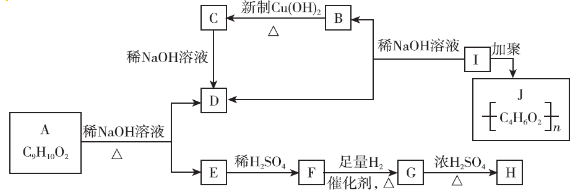
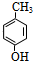 ��
��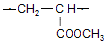 ��
��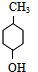 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$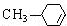 +H2O��
+H2O�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| t��min�� | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| N��Cl2��/10-3��mol/L�� | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
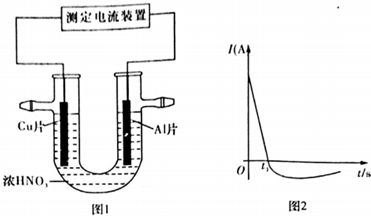
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ܵ�������Ƚ�ʱ��KspС�ģ��ܽ�����һ��С | |
| B�� | ��ʹ��Һ��ij���ӳ�����ȫ������ij�����Ӧ����Խ��Խ�� | |
| C�� | ��ν������ȫ�����ó���������Һ�е�ijһ���ӳ��� | |
| D�� | ����֪Ksp��CaCO3����Ksp��CaC2O4������ʹCa2+��������ȫ��ѡ��Na2CO3��������Ч����Na2C2O4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3����������� | |
| B�� | ����ʪ��ĺ�ɫʯ����ֽ���鰱�� | |
| C�� | ������ζ���ˮ������Һ������ʱ��c��NH4+��=c��Cl-�� | |
| D�� | ����ʱ��0.1mol•L-1NH4Cl��Һ��ˮϡ�ͣ�$\frac{c��N{H}_{4}^{+}��}{c��N{H}_{3}•{H}_{2}O��•c��{H}^{+}��}$��ֵ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com