
| A. | ⅢA族的B和Al都能形成+3价的化合物 | |
| B. | ⅤA族的N和P都能形成-3价的化合物 | |
| C. | ⅠA族的Na和K都能形成+1价的化合物 | |
| D. | ⅦA族的F和Cl都能形成+7价的化合物 |
分析 A.ⅢA族的最外层电子数为3,最高价为+3价;
B.ⅤA族的最外层电子数为5,最低价为-3价;
C.IA族的最外层电子数为1,最高价为+1价;
D.ⅦA族的F只有负价.
解答 解:A.ⅢA族的最外层电子数为3,最高价为+3价,则B和Al都能形成+3价的化合物,故A正确;
B.ⅤA族的最外层电子数为5,最低价为-3价,则N和P都能形成-3价的化合物,故B正确;
C.IA族的最外层电子数为1,最高价为+1价,则Na和K都能形成+1价的化合物,故C正确;
D.ⅦA族的F只有负价,而Cl能形成+7价的化合物,故D错误;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握原子结构、元素的性质为解答的关键,侧重分析与应用能力的考查,注意F只有负价,题目难度不大.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇、乙醛和乙酸都可以与钠反应生成氢气 | |
| B. | 95%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 乙炔和乙烯都可以使溴的四氯化碳溶液褪色 | |
| D. | 福尔马林除了可用于保存生物标本,也可用于食品的保鲜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉中的有效成分为次氯酸钙,在空气中可以长时间放置而不变质 | |
| B. | 二氧化硅是将太阳能转变为电能的常用材料 | |
| C. | 美国纽约冬季城市供暖使用的主要能源是天然气,天然气属于不可再生能源 | |
| D. | 虎门销烟中用到了大量的生石灰,将生石灰投入销烟池的海水中,海水开始翻腾,这是一个物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验操作 | 现象 | 解释或结论 |
| A | 在浓硫酸中加入过量的铁粉,充分反应后滴入KSCN溶液 | 溶液呈红色 | H2SO4将Fe氧化为Fe3+ |
| B | 将苯、溴水混合后加入大试管加热 | 试管底部产生油状物 | 苯发生了取代反应生成了溴苯 |
| C | KIO3溶液中加入HI溶液并加入淀粉 | 溶液变蓝色 | 氧化性:KIO3>I2 |
| D | Cl2通入品红溶液中 | 溶液褪色 | Cl2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 破坏臭氧层 | 化石燃料的燃烧 |
| B | SO2 | 温室效应 | 汽车尾气的排放 |
| C | NO2 | 光化学烟雾 | 工厂废气的排放 |
| D | CO | 酸雨 | 汽车尾气和化石燃料的不完全燃烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
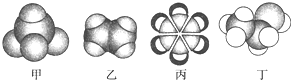
| A. | 甲能使酸性高锰酸钾溶液褪色 | |
| B. | 乙可与溴水发生加成反应使溴水褪色 | |
| C. | 丙中的碳碳键是碳碳单键和碳碳双键交替结合 | |
| D. | 丁不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
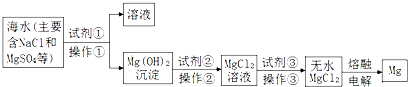
| A. | 试剂①可以选用的试剂是熟石灰,操作①的方法是过滤 | |
| B. | 试剂②可以选用的试剂是盐酸 | |
| C. | 操作③是直接将MgCl2溶液加热蒸发得到无水MgCl2晶体 | |
| D. | 无水MgCl2在通电时发生电离,电解后得到单质Mg. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
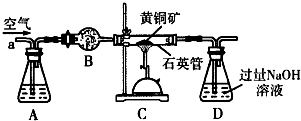

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com