
�л����ת�������������������������ŷdz���Ҫ�����á�
(1)����CH4ȼ��ԭ����CH4����������ȼ�ϵ�أ���صĵ������Һ��KOH��Һ�����й���CH4��ȼ�ϵ��˵������ȷ��Ϊ ��(����ĸ)
A��������Ӧ��O2��2H2O��4e����4OH��
B��������Ӧ��CH4��10OH����8e���� ��7H2O
��7H2O
C������һ��ʱ����Һ��KOH�����ʵ�������
D���ŵ�ʱ��Һ�е�OH���������ƶ�
��2�����������У�����ͨ����ϩ�ӳɷ�Ӧ�õ����� ������ţ���
a��CH3CH3 b��CH3CHCl2 c��CH3CH2OH d��CH3CH2Br
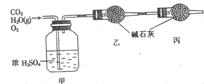
��3����״���£�1.68 L��ɫ��ȼ��������������������ȫȼ�գ���������CO2��H2O������ʣ���O2ȫ��ͨ����ͼ��ʾ��װ�ã��õ����±����е�ʵ�����ݣ��������ɵ�����ȫ�������գ���
| ʵ��ǰ | ʵ��� | |
| ������ / g | 101.1 | 103.8 |
| �ҵ����� / g | 82.0 | 88.6 |
����ʵ��������գ�
����ԭ�����ǵ�һ��̬����ͨ�������ƶ����ķ���ʽ ��
����ԭ���������������ʵ���������Ļ�������ֻ��һ����������д�����ǵķ���ʽ(ֻҪ��д�����ܵ�һ��) ��
��4�� ij�о���С��Ϊ��̽��ʯ����(17��̼���ϵ�Һ̬���������)�ֽ����������ϩ���ڣ��������ͼ��ʵ�鷽�������й���ʵ�����������ȷ���� �� ��
 A�����ɵ�����Ҳ����ͨ��������Ȼ�̼��Һ�л����Ը��������Һ��
A�����ɵ�����Ҳ����ͨ��������Ȼ�̼��Һ�л����Ը��������Һ��
B�����Ƭ����Ҫ�����Ƿ�ֹʯ���ͱ��У�����Σ��
C��ʢ��ˮ���Թ���Һ��ɫ��Ҫ����Ϊ��ϩ����ˮ����
D������ȼ���ɵ����壬�������䴿��
 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ��ó�����ˮ�Ȼ����ڳ�ѹ�����²�ͬ�¶�ʱ���ܶ�Ϊ
| t���棩 | 200 | 400 | 600 | 800 |
| �ѣ�g/L�� | 6.881 | 4.236 | 2.650 | 1.517 |
| ����Ħ�������L/mol�� | 38.8 | 55.2 | 71.6 | 88.0 |
�ɼ���400��ʱ��ˮ�Ȼ���������ʽ�Ļ�ѧʽΪ
A��AlCl3 B��Al2Cl6 C��AlCl3��Al2Cl6 D��Al3Cl9��Al2Cl6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����õ���ʽ��ʾ���γɹ�����ȷ����(����)
A��H ��
��

 �D��H��[
�D��H��[

 ]��
]��
B��Na ��
��

 �D��Na
�D��Na


C. Mg
Mg ��2
��2

 �D��Mg2��[
�D��Mg2��[

 ]��[
]��[

 ]��
]��
D. O
O  ��
�� C
C ��
�� �D��
�D�� ��
�� ��C��
��C�� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����л���ṹ��ʽ��д�������� �� ��
A��CH3(CH2)3CH3 B��CH3C(CH3)2CH2CH3
C��CH3(CH2)2C(CH3)3 D��CH3CH(CH3)3CH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֤ij�л�����������Ӧ��ɵ�ʵ�������� �� ��
A. �ⶨ��������������������ȫȼ�պ�����H2O��CO2������
B. ֤����������ȫȼ�պ����ֻ����H2O��CO2
C. �ⶨ������ȼ�ղ�����H2O��CO2�����ʵ����ı�ֵ
D. �ⶨ��������C��H������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10.6 g Na2CO3����ˮ���1 L��Һ
(1)����Һ��Na2CO3�����ʵ���Ũ��Ϊ__________����Һ��Na�������ʵ���Ũ��Ϊ__________��
(2)�����Һ�м���һ����NaCl���壬ʹ��Һ��Na�������ʵ���Ũ��Ϊ0.4 mol·L��1(������Һ�������)�����NaCl������Ϊ__________��Cl�������ʵ���Ũ��Ϊ________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������Ҫ2 mol·L��1��Na2CO3��Һ950 mL������ʱ������ΪӦ��ѡ�õ�����ƿ�Ĺ��ͳ�ȡ��̼���������ֱ���________��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��a L Al2(SO4)3��(NH4)2SO4�Ļ����Һ�м���b mol BaCl2��ǡ��ʹ��Һ�е�SO ��ȫ���������������ǿ����ȿɵõ� c mol NH3����ԭ��Һ��Al3����Ũ��(mol·L��1)Ϊ
��ȫ���������������ǿ����ȿɵõ� c mol NH3����ԭ��Һ��Al3����Ũ��(mol·L��1)Ϊ
(����)
A. B.
B. C.
C. D.
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��R��W��5�ֶ�����Ԫ�أ�ԭ�����������������ǿ�������ӻ�����Z2Y���ۻ�����RY3��XW4����֪Y��Rͬ���壬Z��R��Wͬ���ڡ�����˵������ȷ����(����)
A��ԭ�Ӱ뾶��Z>R>W
B��X2W6�����и�ԭ�Ӿ�����8���ӽṹ
C����̬�⻯����ȶ��ԣ�HmW>HnR
D��Y��Z�γɵĻ�������ֻ���ܴ������Ӽ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com