
实验得出,无水氯化铝在常压条件下不同温度时的密度为
| t(℃) | 200 | 400 | 600 | 800 |
| ρ(g/L) | 6.881 | 4.236 | 2.650 | 1.517 |
| 气体摩尔体积(L/mol) | 38.8 | 55.2 | 71.6 | 88.0 |
可见,400℃时无水氯化铝存在形式的化学式为
A.AlCl3 B.Al2Cl6 C.AlCl3和Al2Cl6 D.Al3Cl9和Al2Cl6
科目:高中化学 来源: 题型:
二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是
A.利用金属钠或者金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源: 题型:
医学研究证明,用放射性 I治疗肿瘤可收到疗效,下列有关
I治疗肿瘤可收到疗效,下列有关 I的叙述正确的是( )
I的叙述正确的是( )
A. I是碘的一种同素异形体
I是碘的一种同素异形体
B.  I -与Ag+不发生反应,可共存于同一溶液中
I -与Ag+不发生反应,可共存于同一溶液中
C. I核内的中子数与核外电子数之差为29
I核内的中子数与核外电子数之差为29
D. I位于元素周期表中第4周期ⅦA族
I位于元素周期表中第4周期ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量大,而且没有铅污染。其电池反应为2Zn+O2==2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是 ( )
A.锌为正极,空气进入负极反应 B.负极反应为Zn-2e-==Zn2+
C.正极发生氧化反应 D.电解质溶液可以是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
通过复习总结,你认为下列对化学知识概括合理的是
A.能跟酸反应的氧化物,都是碱性氧化物
B.凡具有正四面体结构的分子中,其键角均为109°28′
C.有新单质生成的化学反应一定都是氧化-还原反应
D.核外电子总数相同的原子,一定是同种元素的原子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于砷(As)元素的叙述中,正确的是
A.第一电离能:As<Se,电负性As<Se
B.在AsCl3分子中,砷和氯原子核外电子数均为8
C.砷酸的酸性比亚砷酸强,且砷酸钠溶液呈碱性
D.AsH3的VSEPR模型为三角锥形,其中As原子采取sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的A、B、C、D、E、F、G七种前四周期元素(稀有气体除外),常温下,有三种元素对应的单质呈气态,C与D同族。其中A原子核外有六种不同运动状态的电子,C为地壳中含量做多的元素,F的简单离子是同周期主族元素形成的简单离子中氧化性最弱的,G的基态原子的最外能层只有一个电子,其他能层均已充满电子。
(1)电负性越大的原子,对键合电子的吸引能力越强,通常对应元素化合价呈现负价。根据B、C、D、E四种元素形成的常见化合物的化合价,确定电负性最大的元素,写出其基态原子的电子排布图 。
(2)甲是由B元素等非金属元素组成的离子化合物,甲可由E的氢化物溶液与电解质乙溶液反应生成,写出该反应的离子方程式 。
(3)A元素可形成多种单质,一种晶体结构如图一所示,该晶体与熔融的F单质相互作用,形成某种青铜色的物质(其中的元素F用“●”表示),原子分布如图二所示,该物质的化学式为 。另一种的晶胞如图三所示,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为___________g·cm-3(保留两位有效数字)。
 图一 图二 图三 图四
图一 图二 图三 图四
(4)G元素形成的单质,其晶体的堆积模型为________,G的醋酸盐晶体局部结构如图四,该晶体中含有的化学键是________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)E和F与不同价态的G可组成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均是由G和E两元素形成的无限长链结构(如下图),已知其中一种化合物的化学式为FGE3,另一种的化学式为 。
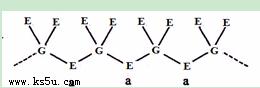
(6)若物质F2D3是一种含有非极性共价键的离子化合物,各原子最外层都满足8e-稳定结构,请你写出该化合物阴离子的电子式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组指定的元素,不能形成AB2型化合物的是( )。
A.2s22p2 和2s22p4 B. 3s23p4 和2s22p4
C.3s2和2s22p5 D. 3s1和3s23p5
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物的转化和性质在生产和生活中有着非常重要的作用。
(1)利用CH4燃烧原理,CH4可用于制造燃料电池,电池的电解质溶液是KOH溶液。下列关于CH4的燃料电池说法中正确的为 。(填字母)
A.正极反应:O2+2H2O+4e-=4OH-
B.负极反应:CH4+10OH--8e-= +7H2O
+7H2O
C.工作一段时间后,电解液中KOH的物质的量不变
D.放电时溶液中的OH-离子向负极移动
(2)下列物质中,可以通过乙烯加成反应得到的是 (填序号)。
a.CH3CH3 b.CH3CHCl2 c.CH3CH2OH d.CH3CH2Br
(3)标准状况下,1.68 L无色可燃性气体在足量氧气中完全燃烧,将产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收)。
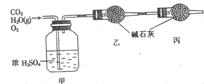
| 实验前 | 实验后 | |
| 甲的质量 / g | 101.1 | 103.8 |
| 乙的质量 / g | 82.0 | 88.6 |
根据实验数据填空:
①若原气体是单一气态烃,通过计算推断它的分子式 。
②若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出可能的一组) 。
(4) 某研究性小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如图的实验方案,下列关于实验的叙述不正确的是 ( )
 A.生成的气体也可以通入溴的四氯化碳溶液中或酸性高锰酸钾溶液中
A.生成的气体也可以通入溴的四氯化碳溶液中或酸性高锰酸钾溶液中
B.碎瓷片的主要作用是防止石蜡油暴沸,带来危险
C.盛溴水的试管溶液退色主要是因为乙烯被溴水氧化
D.若点燃生成的气体,需先验其纯度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com