
| A. | 5.4 g | B. | 3.6g | C. | 2.7 g | D. | 1.8 g |
分析 根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,若Al都完全反应,则生成氢气应相等,而应结束后测得生成的气体体积比为甲:乙=3:4,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知酸与金属反应时酸不过量,碱与金属反应时碱过量,结合方程式计算解答.
解答 解:根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,若Al都完全反应,则生成氢气应相等,而应结束后测得生成的气体体积比为甲:乙=3:4,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知酸与金属反应时酸不过量,碱与金属反应时碱过量,
盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,则:
2Al+6HCl═2AlCl3+3H2↑
6 3
0.3mol x
解得x=$\frac{0.3mol×3}{6}$=0.15mol,
则碱与金属铝反应生成的氢气的物质的量为0.15mol×$\frac{4}{3}$=0.2mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,则:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.2mol
解得y=$\frac{0.2mol×2}{3}$=$\frac{0.4}{3}$mol,
则铝的质量为$\frac{0.4}{3}$mol×27g/mol=3.6g,
故选:B.
点评 本题考查化学反应方程式的计算,关键是判断反应中酸、碱是否足量,难度中等.


科目:高中化学 来源: 题型:解答题
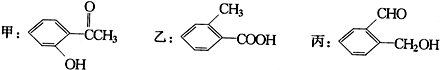
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 工业合成氨时选择铁做催化剂能极大加快反应速率 | |
| C. | 向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 | |
| D. | 工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 | |
| B. | 制取并用排水法收集氧气结束后,应立即停止加热 | |
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 金属钠着火,应该立即用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 2Br-+Cl2═Br2+2Cl- | |
| C. | 2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含元素化合价升高的物质是还原剂 | |
| B. | 氧化剂失去电子,所含元素的化合价升高 | |
| C. | 作氧化剂的物质不能作还原剂 | |
| D. | 化合价降低,失去电子的物质是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应都是氧化还原反应 | |
| B. | 复分解反应都不是氧化还原反应 | |
| C. | 在反应 2H2S+SO2=3S+2H2O中,还原剂是SO2 | |
| D. | 在一个氧化还原反应中,同一种反应物不可能既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质每个分子中含有25个原子 | |
| B. | 该物质中碳、氢、钾、氧元素间的质量比是6:7:3:8 | |
| C. | 该物质是由原子直接构成的 | |
| D. | 该物质是由碳、氢、钾、氧四种元素组成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某卤代烃与NaOH溶液共热后滴加AgNO3溶液,产生白色沉淀,说明该卤代烃为氯代烃 | |
| B. | 向装有铁粉的烧瓶中加入苯、溴水,可以制取溴苯 | |
| C. | 将乙醇与浓硫酸在170℃时共热产生的气体直接通入KMnO4酸性溶液中,溶液褪色,并不能说明乙醇与浓硫酸在170℃时共热产生了乙烯 | |
| D. | 向苯酚的浓溶液中滴加几滴稀溴水,可以观察到产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com