
����Ŀ���������ǽ������ϵ����ǣ���������������Լռ�ؿ�������90%���ϡ�
��1�������оƬ��̫���ܵ�ص���Ҫ�ɷ���____________�����ά����Ҫ�ɷ���______________��
��2������ʦ�������������̲������÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
��3����ҵ�Ͽ�����ˮ���������ᷴӦ�Ʊ�����������һ����ˮ�����ɵõ��轺��д��ˮ���������ᷴӦ�����ӷ���ʽ___________________________________________��
��4����ʯ����Ҫ�ɷֻ��������ڹ����Σ�������Ҫ�ɷ�ΪNaAlSi2O6�������ʾΪ��������ʽΪ_________________________��
��5���ߴ��ȵ�����������з����Ʊ�:
SiO2 ![]() Si(��)
Si(��) ![]() SiHCl3
SiHCl3 ![]() Si(��)
Si(��)
д������ٵĻ�ѧ����ʽ___________________________________________________��
����ڵIJ��ᆳ��������õ���SiHCl3(�е�33.0��)�к���������SiCl4(�е�57.6��)���ᴿSiHCl3��Ҫ������������_________��
��������Ҫ����ˮ���������½��У��������������£������в���ȫ���������ʹ��Ʒ�л�������____________��
���𰸡� Si SiO2 4HF+ SiO2 = SiF4 ��+ 2H2O SiO32��+2H+=H2SiO3�����壩 Na2O��Al2O3��4SiO2 2C+ SiO2 ![]() Si+ 2CO�� ���� SiO2
Si+ 2CO�� ���� SiO2
��������
��1��Si�ǰ뵼�壬���������оƬ��̫���ܵ�ص���Ҫ�ɷ֣����ά����Ҫ�ɷ���SiO2���Ա����Ϊ��Si SiO2 ��
��2������ʦ�������������̲���������Ϊ������SiO2��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ
4HF+ SiO2 = SiF4 ��+ 2H2O��
��3����ҵ�Ͽ�����ˮ���������ᷴӦ�Ʊ�����������һ����ˮ�����ɵõ��轺��д��
ˮ������Na2SiO3�������ᷴӦ�����ӷ���ʽΪ��SiO32��+2H+=H2SiO3�����壩��
��4��.������Ҫ�ɷ�ΪNaAlSi2O6�������ʾΪ��������ʽΪ: Na2O��Al2O3��4SiO2��
(5).����ٵĻ�ѧ����ʽΪ2C+ SiO2 ![]() Si+ 2CO�� ��
Si+ 2CO�� ��
����ڵIJ��ᆳ��������õ���SiHCl3(�е�33.0��)�к���������SiCl4(�е�57.6��)���������߷е㲻ͬ�������������롣�ᴿSiHCl3��Ҫ�����������ǣ�����
�������Ҫ����ˮ���������½��У��������������£������в���ȫ���������ʹ��Ʒ��
���� Si��O2�ڸ��µ������»�����SiO2���ʡ����Դ�Ϊ��SiO2 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�Ϊ�������ʻ����ǵ���Һ������AΪ����ɫ���ݣ�C��X��Ϊ��ɫ���壬ZΪdz��ɫ��Һ��DΪһ�ֳ�����ǿ���������֮���ת����ϵ����ͼ�����û�ѧ����ش����⡣�����ֲ�����ʡ�ԣ�

��1��д���������ʵĻ�ѧʽ��A_______ D__________
��2��A��SO3��g���ķ�Ӧ������A��X�ķ�Ӧ����д��A��SO3��g����Ӧ�Ļ�ѧ����ʽ������÷�Ӧ����ת�Ƶķ������Ŀ��____________________________________��
��3������Eת��Ϊ����F������Ϊ___________________________________________����ѧ����ʽΪ____________________________________________��
��4����10gD����Һ��ͨ��һ������X����ȫ��Ӧ���ڵ��������������ᾧ�����յõ�14.8g���塣���ù����к��е����ʼ������ʵ���֮��Ϊ_____________�� ������ʾ����n(A)�Un(B)=a�Ub�������������ᾧ�ڵ��������½��е����ɣ�___________���ñ�Ҫ���ֻش�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���������ͼ���ʼ�ת����ϵ�����ʼ�ķ�Ӧ��Ϊһ��ת������ѡ����


A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�ͭ���Ȼ�þ�Ļ����Һ�У�������������ۣ���ַ�Ӧ����ˣ�������ֽ�ϵ�������( )
A.FeB.CuC.Fe��CuD.Mg��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�еķ�Ӧ��MnO4-��5Fe2����8H��=5Fe3����Mn2����4H2O�����д�ʩ��ʹ��ѧ��Ӧ������ߵ���( )
A.��ˮ
B.����ͬŨ��FeSO4������
C.����Һ�еμ�ϡ����
D.��������KMnO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe(OH)3����װ��U���У�����ʯī�缫����ֱ����Դ��ͨ��һ��ʱ����ֽ�����������������ƶ������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᣨH3PO2����һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺
��1��H3PO2��һԪ��ǿ�ᣬд������뷽��ʽ�� ��
��2��H3PO2�У���Ԫ�صĻ��ϼ�Ϊ ��
��3��NaH2PO2�����λ�����ʽ�Σ�����Һ���ԣ��������ԡ����ԡ����������ԣ���
��4��H3PO2Ҳ����ͨ�����ķ����Ʊ�������ԭ����ͼ��ʾ����Ĥ����Ĥ�ֱ�ֻ���������ӣ�������ͨ������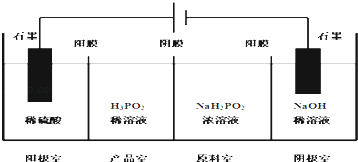
��д�������ĵ缫��Ӧʽ ��
�ڷ�����Ʒ�ҿɵõ�H3PO2��ԭ�� ��
�����ڲ��á����ҵ����������Ʊ�H3PO2 �� �������ҵ����������������ҵ�ϡ������H3PO2ϡ��Һ���棬����ȥ���������Ʒ��֮�����Ĥ���Ӷ��ϲ������������Ʒ�ң���ȱ�������ʣ������ʲ�����ԭ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D����ѧ��ѧ�������ʣ�������һ����������A+B��C+D��ת����ϵ��
��1����AΪ��������BΪ���������÷�Ӧ��һ����;��_______________��
��2����A��һ����ʹ��ɫʯ����Һ���������壬�Ҹ÷�Ӧ�ǹ�ҵ����ȡ�������Ҫ��Ӧ֮һ���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ____________________________��
��3����A�ǵ���ɫ��ĩ����������������CΪǿ���÷�Ӧ�����ӷ�Ӧ����ʽΪ__________��
��4����A��һ����ʽ�Σ�����ΪʳƷ���������е����ɼ���A��B��D����ˮʱ���ʼ�������÷�Ӧ�����ӷ�Ӧ����ʽΪ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӻ�������Ʊ�1��4�����������������������й������йص�8����Ӧ���������������ﶼ����ȥ���� 
��1�������١���8������������ȡ����Ӧ����������ţ���ͬ����������ȥ��Ӧ���������ڼӳɷ�Ӧ���� ��
��2��д���������ʵĽṹ��ʽ��
B �� C �� D ��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
�� ��
�� ��
�� ��
�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com