
| A����֪�����ۻ���Ϊ6.0 kJ/mol�������������Ϊ20 kJ/mol������1 mol������2 mol ��������ۻ�����ȫ�����ƻ���������������ֻ���ƻ�����15%����� |
| B��SO2��SO3���Ǽ��Է��� |
| C��ʵ���û����飨l��������ϩ��l���ͱ���l���ı�ȼ���ȷֱ�Ϊ-3916 kJ/mol��-3747 kJ/mol��-3265 kJ/mol������֤���ڱ������в����ڶ�����̼̼˫�� |
| D���������еĹ����ǽ������չ��Ӷ�����ԾǨ�����ض������ĹⲨ |
| 6KJ |
| 40KJ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1mol?L-1NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
| B����0.1mol?L-1Na2CO3��Һ�У�c��OH-��-c��H+���Tc��HCO4-��+2c��H2CO3�� |
| C����0.2mol?L-1NaHCO3��Һ�м�������0.1mol?L-1NaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� |
| D�������£�pH=7��CH3COONa��CH3COOH�����Һ��c��Na+��+c��CH3COO-���Tc��H+��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��O2��O3��Ϊͬλ�� |
| B��O2��O3���ת���������仯 |
| C������ͬ���¶���ѹǿ�£��������O2��O3������ͬ�ķ����� |
| D�������ʵ�����O2��O3������ͬ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��28�� | B��32�� |
| C��40�� | D��48�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Է������������ݣ��Ʋ��Ҵ��ͱ���е����Ըߵ� |
| B�������ܽ�ȵ����ݣ�ѡ�����ؽᾧ�ķ����ɽ��ֱ������ᴿ |
| C�����ݷе�����ݣ��ж��÷���ķ�����ʯ���л�ȡ���ͺ�ú�͵� |
| D������ȼ���ȵ����ݡ��Ȼ�ѧ����ʽ��˹���ɣ��ɼ���һЩ��Ӧ�ķ�Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ�Ӱ뾶��С��Z��Y��X��W |
| B��Y��Z����Ԫ�ص��������Ӧ��ˮ��������Ϊ��Y��Z |
| C��X��Y��Z����Ԫ�صĵ��ʾ��������������л�ԭ�� |
| D��W��Y��Z����Ԫ���γɵ���̬�⻯�������ȶ�����Z����̬�⻯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��A��B��D��E����Ԫ�����γɵ���ۺ�������D��������ǿ |
| B���γɵļ������Ӱ뾶�Ĵ�С˳��Ϊ��C��B��D��E |
| C��D��E��F����Ԫ���γɵĵ����ж����й��ۼ� |
| D��1 mo1A��B��CԪ�صļ��⻯���ж�����10 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
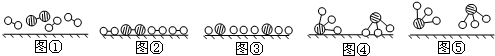
 ��
��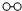 ��
��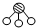 �ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������森�ֱ�д��ͼ�ڡ��ۡ�ͼ�ۡ��ܱ�ʾ�ı仯����
�ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������森�ֱ�д��ͼ�ڡ��ۡ�ͼ�ۡ��ܱ�ʾ�ı仯����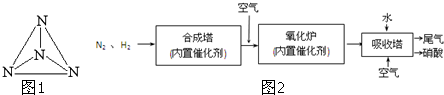
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A�����ת��3mol e-ʱ�������Ͽ��Ƶ�KIO3 107 g |
| B�����ʱ��ʯī������������������� |
| C�����ʱ�������缫��Ӧʽ��I--6e-+3H2O�TIO3-+6H+ |
| D���������е������Һ��pH��С |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com