
下列与化学有关的叙述正确的是
A.铜锌原电池中铜为负极
B.0.1 mol N2与0. 3 mol H2在一定条件下反应达到平衡时,生成0.2 mol氨
3 mol H2在一定条件下反应达到平衡时,生成0.2 mol氨
C.1 mol·L-1 AlCl3溶液中,铝离子物质的量浓度为1 mol·L-1
D.18 g H2O中含1 mol氧原子
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B.0.1 mol丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2 L苯中含有分子的数目为0.5NA,
D.在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是( )
A.23 g钠在氧气中完全燃烧失电子数为0.5NA
B.1 L 2 mol·L-1的MgCl2溶液中含Mg2+数为2NA
C.标准状况下,11.2 L的SO3所含分子数为0.5NA
D.室温下,8 g甲烷含有共价键数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件下,两瓶气体所含原子数一定相等的是
A.同质量、不同密度的N2和 CO
CO
B.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H6
D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数约为6.02×1023 mol—1,下列叙述中正确的是
A.常温常压下,18.0g 重水(D2O)所含的电子数约为10×6.02×1023
B.室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约 为3×6.02×1023
为3×6.02×1023
C.标准状况下,22.4L 甲苯所含的分子数约为6.02×1023
D.标准状况下,a L 甲烷和乙烷混合气体中的分子数约为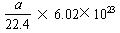
查看答案和解析>>
科目:高中化学 来源: 题型:
已知①丙烷②正丁烷③异丁烷④2-甲基丁烷⑤己烷,上述物质的沸点按由低
到高的顺序排列的是
A.①③②④⑤ B.⑤④③②① C.①②③④⑤ D.⑤①②④③
查看答案和解析>>
科目:高中化学 来源: 题型:
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发
生取代反应。由此可以断定原气态烃是(气体体积均在相同条件下测定)
A.乙炔 B.丙炔 C.丁炔 D.丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
W克下列物质电火花引燃后的产物通过足量的Na2O2后,固体增重大于W克的是
A.CO与H2的混合气体 B.CH3CH2OH C.HCOOH D.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G、H均为有机化合物。

根据上图回答问题:
⑴ D的化学名称是 。
⑵ D在一定条件下与O2反应生成H,H可发生银镜反应。H发生银镜反应的化学方程式_____________________________________________。
⑶ B的分子式是 ,A的结构简式是 ,反应①的反应类型是 。
⑷ 符合下列3个条件的B的同分异构体的数目有_______个。
①含有邻二取代苯环结构 ②与B有相同官能团 ③不与FeCl3溶液发生显色反应
写出其中一个同分异构体的结构简式___________________。
⑸ G是重要的工业原料,用化学方程式表示G的一种重要的工业用途
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com