
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
【答案】C
【解析】试题分析:加入过量的稀盐酸有气体产生,说明CO32-、SO32-至少有一种,气体甲中CO2、SO2至少有一种。镁离子、铝离子与CO32-、SO32-均不能大量共存,一定不存在镁离子、铝离子;加入过量的盐酸有沉淀,说明一定有硅酸根离子,沉淀甲是硅酸。无色溶液中加入过量氨水有沉淀生成,该沉淀只能是氢氧化铝沉淀,说明此时溶液中存在铝离子。由于原溶液中的铝离子一定不存在,所以该铝离子是偏铝酸根离子和盐酸反应生成的,则一定存在偏铝酸根离子。根据溶液的电中性可知一定含有K+离子。A、根据以上分析可知气体甲不一定是纯净物,A错误;B、根据以上分析可知沉淀甲是硅酸,不可能是硅酸镁,B错误;C、根据以上分析可知原来溶液中K+、AlO2-和SiO32-一定存在,C正确;D、根据以上分析可知硫酸根离子不能确定是否存在,CO32-可能存在,D错误,答案选C。


科目:高中化学 来源: 题型:
【题目】NaClO2广泛用于造纸工业、污水处理等,其漂白能力是漂白粉的4~5倍,工业上用C1O2气体制NaClO2的工艺流程如下:

己知:NaClO2饱和溶液在低于38℃时析出NaC1O2·3H2O,高于38℃时析出NaClO2
下列说法不正确的是
A. 吸收器中生成NaClO2的离子方程式:2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O
B. 流程中的结晶、过滤操作应该是蒸发结晶、趁热过滤
C. 提高吸收器中的反应温度可以提高反应速率,也提高反应物的利用率
D. 发生器中反应结束后,向其中通入一定量空气的目的是驱赶出ClO2,使其被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式__________________。
(2)利用____(写化学式,下同)的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是__________________。
(3)“净化除杂”需先加H2O2溶液,作用是__________________。
(4)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中只可能溶有NH![]() 、K+、Al3+、Mg2+、HCO
、K+、Al3+、Mg2+、HCO![]() 、Cl-、I-、MnO
、Cl-、I-、MnO![]() 、SO
、SO![]() 等离子中的几种离子。为分析其组成,现进行如下实验:
等离子中的几种离子。为分析其组成,现进行如下实验:
①取10 mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03 mol白色沉淀甲。
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生。
③另取10 mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加入NaOH的物质的量为0.03 mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224 L(假设丙全部逸出),最后沉淀完全溶解。
下列推断正确的是( )
A. 仅有实验①可推出肯定含有SO![]() ,不含Cl-
,不含Cl-
B. 该无色溶液肯定含有NH![]() 、K+、Al3+、SO
、K+、Al3+、SO![]()
C. 该无色溶液中肯定不含K+、Mg2+、HCO![]() 、Cl-、MnO
、Cl-、MnO![]() 、I-
、I-
D. 不能确定该无色溶液是否含有K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
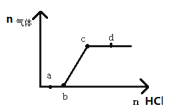
A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:H+、Fe3+、MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d点对应的溶液中:S2-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②![]() 、
、![]() 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答:
(1)HmDm的结构式___________________。
(2)![]() 、
、![]() 的还原性强的为:_________,能证明其还原性强弱的离子方程式为_______。
的还原性强的为:_________,能证明其还原性强弱的离子方程式为_______。
(3)将E的单质通入A与D形成的化合物的水溶液中,其化学方程式为:_________________。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的化学方程式__________________________________。在该溶液中溶质中含有的化学键类型是____________。
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)除去自来水中的Cl-等杂质得到蒸馏水,选择装置__________(填序号),操作名称_________;实验中加入沸石的目的是____________;
(2)用四氯化碳提取出碘水中的I2,选择装置_________(填序号),操作名称_________;静置分层时,下层是______溶液,呈________色。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a mol Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250 ℃,使其充分反应,当排出O2和H2O(g)的物质的量之比为1∶1 时,a∶b为
A.1∶1 B.1∶2 C.2∶3 D.2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com